北京时间2019年11月2日,国际学术期刊《自然—遗传学》更新了7篇论文。机器人“小柯”对其进行了精心写作。
其中两项成果为中国农业科学院联合国内外优势单位,完成的瓜类作物基因组研究。
北京市农林科学院许勇团队、中国农科院郑州果树研究所刘文革团队、美国康奈尔大学BoyceThompson研究所费章君团队和中国农科院深圳农业基因组研究所黄三文团队等合作完成了新的西瓜基因组图谱绘制。2019年11月1日,国际学术期刊《自然—遗传学》在线发表了该研究成果。研究人员报道了一个改进的西瓜参考基因组和414个代表西瓜属所有现存物种的全基因组重测序。群体基因组分析揭示了西瓜属的进化历史,表明了Citrullus amarus与含有Citrullus lanatus和Citrullus lanatus谱系的独立进化。研究人员发现,在形成、驯化和改良过程中,影响西瓜果实大小的不同基因座受到了选择。在甜西瓜的祖先中产生的非苦等位基因主要固定在C. lanatus中。果肉甜度的选择始于C.lanatus的祖先,并通过控制棉子糖分解代谢和糖运输的基因座在现代育种继续进行。果肉的颜色和糖分积累可能是通过包括糖转运蛋白基因在内的共有遗传成分共同进化而来。这项研究提供了宝贵的基因组资源,并阐明了西瓜的物种形成和育种历史。据了解,甜西瓜的水果特性很大程度上是人类选择的结果。https://www.nature.com/articles/s41588-019-0518-4 中国农科院深圳农业基因组研究所黄三文团队、中国农科院郑州果树研究所徐永阳团队以及西班牙巴塞罗那食品科学院JordiGarcia-Mas团队等合作绘制了甜瓜的综合性基因组变异图谱,并鉴定了多个影响其农艺性状的驯化事件和基因座。研究论文11月1日在线发表于《自然—遗传学》。研究人员报道了从1175个品系的重测序中得出的甜瓜基因组变异的综合图谱,其代表了该物种的全球多样性。结果表明,甜瓜中发生了三个独立的驯化事件,其中两个发生在印度,一个发生在非洲。研究人员检测到两个独立的驯化事件,从而在甜瓜育种过程中产生了不同特征的两个亚种melo和agrestis。对16个农艺性状的全基因组关联研究确定了208个与果实质量、品质和形态特征显著相关的基因座。这项研究揭示了甜瓜的驯化历史,并为该重要作物的基因组学育种提供了宝贵的资源。据悉,甜瓜是一种经济上重要的水果作物,已经栽培了数千年。然而,其驯化的遗传基础和历史仍然未知。https://www.nature.com/articles/s41588-019-0522-8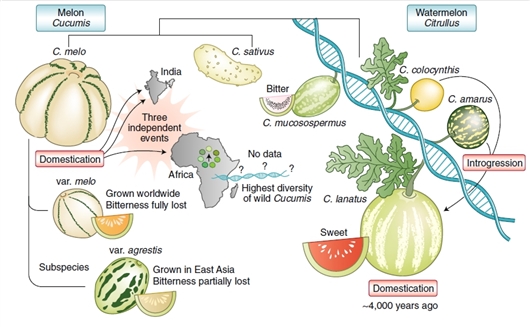
两种葫芦科植物的驯化历史。图片来源:《自然—遗传学》
芬兰赫尔辛基大学Leif Groop研究团队发现,ZnT8蛋白的功能丧失可通过增强胰岛素分泌来预防糖尿病。2019年11月1日,国际学术期刊《自然—遗传学》在线发表了这一研究成果。
据研究人员介绍,SLC30A8基因(编码锌转运蛋白8,ZnT8)中的一种罕见的功能丧失等位基因p.Arg138*,在芬兰西部人群中富集,其可预防2型糖尿病(T2D)。研究人员招募了已鉴定携带者的亲属,结果表明,由于葡萄糖反应性和胰岛素原转化增强,这种保护与更好的胰岛素分泌相关,特别是与具有常见T2D风险等位基因SLC30A8(p.Arg325)基因型的个体相比。在基因组编辑的人类诱导的多能干细胞(iPSC)衍生的β样细胞中,研究人员确定p.Arg138*等位基因由于单拷贝功能不足而导致SLC30A8表达降低。在人β细胞中,与从T2D保护性等位基因p.Trp325人群分离的胰岛细胞相似,SLC30A8的缺失导致葡萄糖反应性增强和KATP通道功能降低。这些数据表明,ZnT8可作为旨在维持T2D中胰岛素分泌能力的治疗靶标。https://www.nature.com/articles/s41588-019-0513-9美国北卡罗来纳大学教堂山分校Hongtu Zhu等研究人员利用19629名个体的全基因组关联分析确定了影响大脑容量的变异,并利用认知和心理健康特征完善了其遗传结构。相关论文在线发表于11月1日的《自然—遗传学》。研究人员使用包括19629名参与者的英国生物银行样本,对101种脑容量表型进行了全基因组关联研究(GWAS)。GWAS鉴定了365个独立遗传变体(显著性阈值超过4.9×10−10),并对多种表型进行了相应调整。一项基于基因的关联研究发现了157个相关基因(124个新基因),而功能基因图谱分析将146个其他基因联系在一起。先前发现的许多遗传变异和基因都与认知和心理健康特征有关。通过全基因组多基因风险评分预测,英国生物银行GWAS结果可以解释其他四项独立研究中超过6%的表型变异(P =3.13×10-24)。总之,这项研究在变体、基因座和基因水平上鉴定了许多新的遗传关联,并加深了我们对大脑体积和其他特征之间的多效性和遗传共构关系的理解。据了解,人脑的体积变化是可遗传的,并且与许多与脑有关的复杂性状有关。https://www.nature.com/articles/s41588-019-0516-6美国哈佛医学院Pradeep Natarajan等研究人员利用静脉血栓栓塞的全基因组关联分析,确定了新的风险基因座以及与动脉血管疾病之间的遗传重叠。该研究成果于2019年11月1日,在线发表于国际学术期刊《自然—遗传学》。研究人员在"百万老兵计划"和英国生物银行中进行了一项全基因组关联研究,测试了约1300万个与静脉血栓栓塞相关的DNA序列变异(26066例和624,053个对照),并对这两项研究进行了荟萃分析,然后进行独立复制多达17672例静脉血栓栓塞病例和167295例对照。研究人员确定了22个以前未知的基因座,使与静脉血栓栓塞相关的基因座总数达到了33个,并随后对其进行精细映射。研究人员为静脉血栓栓塞症建立了全基因组多基因风险评分,其可确定与建立的因子V Leiden p.R506Q和凝血酶原G20210A突变的携带者同等的静脉血栓栓塞风险。这些数据为静脉血栓栓塞的遗传流行病学提供了机制见解,并提示静脉和动脉性心血管疾病之间的重叠比以前想象的要大。据悉,静脉血栓栓塞是导致死亡的重要原因,但其遗传决定因素尚未完全确定。https://www.nature.com/articles/s41588-019-0519-3美国加州大学旧金山分校Melissa Gymrek等研究人员系统性揭示了短串联重复序列(STR)变异对基因表达的影响。相关论文11月1日在线发表于《自然—遗传学》。研究人员利用来自基因型组织表达计划的17个组织的全基因组测序和表达数据,鉴定出28000个STR,其重复数与附近基因(eSTR)的表达有关。研究人员使用了精细映射来量化每个eSTR因果关系的可能性,并表征前1400个精细映射的eSTR。研究人员确定了数百种与已发表的全基因组关联研究信号相关的eSTR,并将特定的eSTR关联到复杂的性状中,包括身高、精神分裂症、炎症性肠病和智力。总体而言,这些结果支持以下假设:eSTR贡献于大量的人类表型;并且这些数据可作为以后研究复杂性状的宝贵资源。据介绍,STR与人类的各种复杂性状有关。但迄今为止,STR对基因表达影响的全基因组相关研究对于检测关联性并对潜在机制提供见解的能力有限。https://www.nature.com/articles/s41588-019-0521-9西班牙Germans Trias i Pujol大学医院与研究所的Lorenzo Pasquali团队揭示了促炎细胞因子对β细胞调节作用,并为1型糖尿病(T1D)的发病机制提供了新的见解。11月1日,《自然—遗传学》在线发表了这一成果。研究人员发现,促炎细胞因子的接触揭示了β细胞调节表观图谱的显著可塑性。通过映射与β细胞转录组、蛋白质组和三维染色质结构变化相关的刺激响应性增强子,研究人员扩展了人类胰岛调节元件的功能。这些数据表明,β细胞对细胞因子的反应是通过诱导新的调控区以及活化调控元件(被胰岛特异性转录因子预先结合)的激活来介导的。研究人员发现,与T1D相关的基因座富含新定位的顺式调控区域,并鉴定了可破坏人类β细胞中细胞因子响应型增强子活性的T1D相关变体。这项研究说明了β细胞如何对促炎环境做出反应,并暗示T1D中刺激响应胰岛增强子的作用。据介绍,T1D早期阶段的特征是局部自身免疫炎症和胰岛素产生性胰腺β细胞的逐步丢失。https://www.nature.com/articles/s41588-019-0524-6http://paper.sciencenet.cn/AInews/
“小柯”是一个科学新闻写作机器人,由中国科学报社联合北大团队研发而成。新闻由“小柯”独立完成,经领域专家和科学编辑双重人工审校和信息补充。“小柯生命”是“小柯”系列学术公众号之一,主要介绍生命科学领域顶级学术期刊最新论文信息。
https://m.sciencenet.cn/blog-3423233-1204918.html
上一篇:
76%!生命科学领域论文“霸占”《科学》版面下一篇:
菜单上要标注“热量”,你就不点奶茶了?

