博文
《核酸研究》:郑杰/陈伟/李丹团队揭示天然免疫RNA受体RIG-I介导的自身免疫疾病新机制
||
2022年5月17日,中国科学院上海药物研究所郑杰课题组联合浙江大学医学院陈伟课题组、浙江大学药学院李丹课题组在《核酸研究》(Nucleic Acids Research)杂志上以Research Article形式在线发表论文——“A loosened gating mechanism of RIG-I leads to autoimmune disorders”。
该研究通过使用生物大分子氢/氘交换质谱(HDX-MS)和单分子磁镊技术(MT),阐释了RIG-I区分自身和非自身RNA以及RIG-IE510V和RIG-IQ517H突变体的基因型-表型梯度决定自身免疫性疾病Singleton-Merten综合征(SMS)临床表型的潜在分子机制。

RIG-I属于RIG-I样受体(RLRs)家族,参与识别病毒RNA并介导I型干扰素参与的免疫反应【1】。RIG-I主要识别具有病原体相关分子模式(PAMP)RNA特征的带有5'-三磷酸或5'-二磷酸修饰的双链、短链RNA。由于多种RNA编辑酶的存在,人类和其他高等真核生物的mRNA在5’端具有7-甲基鸟苷(m7G)帽(Cap0)结构并存在Cap1(N1-2’-O-M)或Cap2(N1-2-2’-O-M)修饰。该2’-O-甲基化修饰可避免自身RNA被RIG-I错误识别。RIG-I功能获得型突变可驱动I型干扰素的升高,从而导致SMS。然而,功能获得型RIG-I突变体的基因型-表型梯度是如何决定SMS临床梯度(轻度和重度表型)的潜在分子机制不清楚【2-5】。
首先研究人员通过氢/氘交换质谱(HDX-MS)对静息状态(apo)RIG-I的研究证明,HEL2i结构域中510和517位点的突变削弱了CARD2-HEL2i界面结合的紧密程度,促进了RIG-I自抑制构象的部分开放,导致一些通常埋在CARD-HEL2i界面的残基变得更加暴露并进行更多的溶剂交换。与apo RIG-IE510V 相比,apo RIG-IQ517H的CARD-HEL2i界面溶剂暴露程度更高(图1A)。研究人员进一步研究PAMP-RNA(5‘ppp RNA)和自身RNA(Cap RNA)对RIG-I溶液构象的影响,并通过HDX-MS监测RIG-I在溶液中的构象变化发现RIG-I可以区分PAMP-RNA和Cap2 RNA,并实现了对RNA的正确校对。然而,RIGIE510V和RIG-IQ517H逐渐丧失了对5’ppp和Cap2 RNA的校正的能力,并伴随着异常的构象变化。
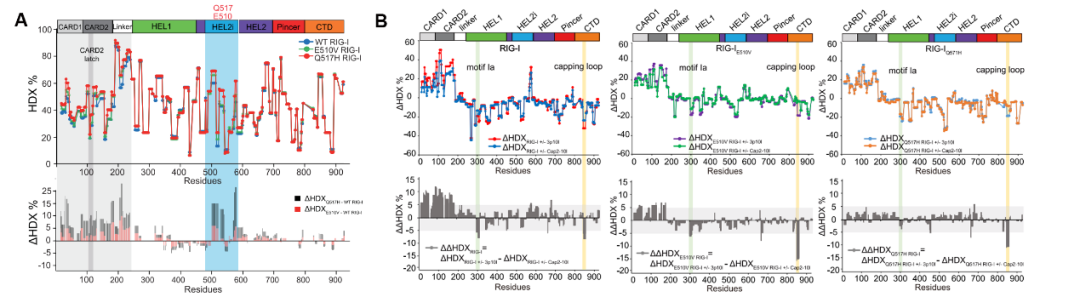
图1:HDX-MS分析RIG-I及功能获得型RIG-I在apo和RNA校对状态的构象变化的差异
研究人员进一步通过单分子磁镊技术(MT)发现相对于RIG-I,RIG-IQ517H功能获得型突变体在初始状态比RIG-I长8 nm,进而显示两种蛋白在初始构象上的差异(图2A-C)。当RIG-I模拟识别PAMP-RNA以及Cap2 RNA时,磁单极拉伸的长度在RIG-I中具有显著的差异,而在RIG-IQ517H中没有显著性差异(图2D-E),进一步证明了RIG-IQ517H失去了对PAMP RNA和Cap2 RNA的区分能力。
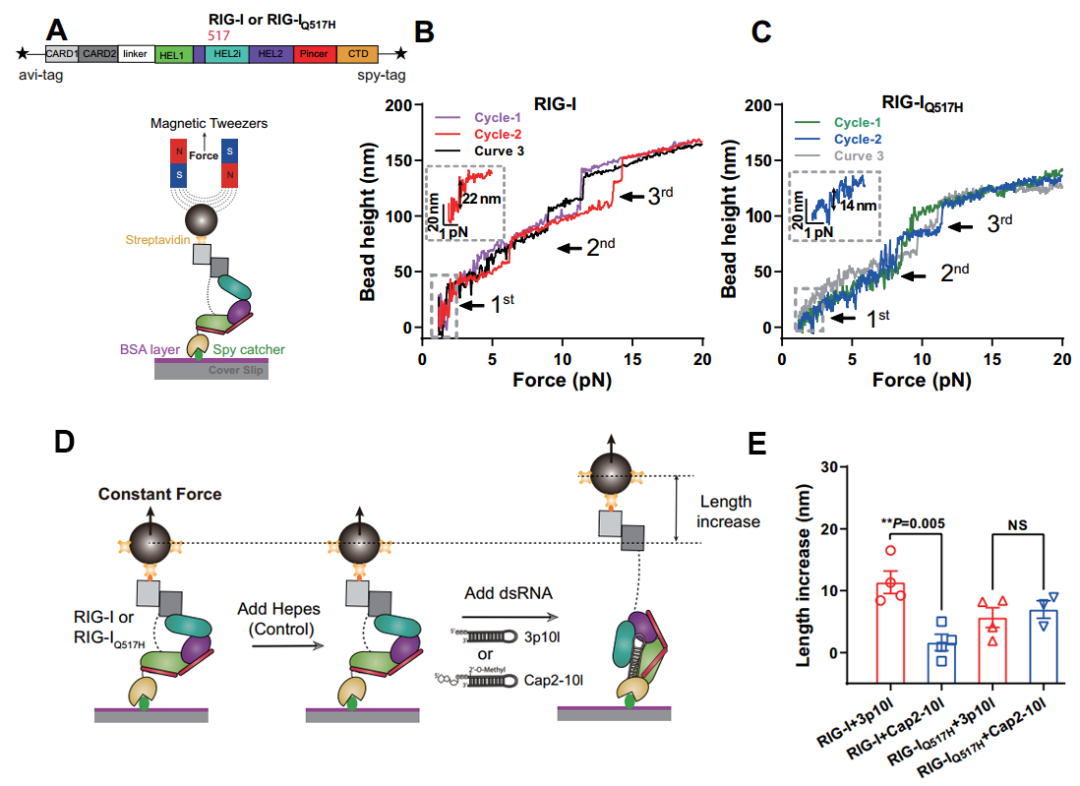
图2:单分子磁镊技术分析RIG-I与突变体静息状态及结合RNA状态的构象差异
综上所述,该研究通过HDX-MS和MT为研究蛋白的动力学及构象变化提供了灵敏的定量方法。该研究阐释了RIG-I区分自身和非自身RNA以及RIG-IE510V 和RIG-IQ517H突变体的基因型-表型梯度决定SMS的临床梯度(轻度和重度表型)的潜在分子机制(图3),同时揭示了RIG-I的HEL2i在协调RNA识别和CARDs信号传导的关键作用。

图3:RIG-I突变体错误识别自身RNA伴随的异常构象变化
浙江大学药学院和中国科学院上海药物研究所联合培养硕士生雷艺璇和浙江大学医学院费攀宇博士为论文的共同第一作者,中国科学院上海药物研究所博士后宋斌和研究生史文佳为论文做出了重要贡献。中国科学院上海药物研究所郑杰研究员、浙江大学医学院陈伟教授、浙江大学药学院李丹副教授为论文的共同通讯作者。该工作得到了新加坡南洋理工大学罗大海教授和中国科学院上海药物研究所罗成研究员的重要支持。
郑杰研究员团队长期专注于基于氢/氘交换质谱(HDX-MS)技术的蛋白质动态调控机制及药物发现方向的研究。相关工作以通讯作者发表在Immunity 2021,Nucleic Acids Res 2022等杂志。欢迎对分子免疫学、药理学、生物大分子质谱等相关背景的学生和博士后加入团队。
详细信息请查阅网站:
http://www.simm.cas.cn/web/rcdw/rczp/kygw/202109/t20210928_6216304.html
相关论文信息:
https://doi.org/10.1093/nar/gkac361
参考文献
1. Rehwinkel, J. and Gack, M.U. (2020) RIG-I-like receptors: their regulation and roles in RNA sensing. Nat Rev Immunol. 2. Jang, M.A., Kim, E.K., Now, H., Nguyen, N.T.H., Kim, W.J., Yoo, J.Y., Lee, J., Jeong, Y.M., Kim, C.H., Kim, O.H. et al. (2015) Mutations in DDX58, which Encodes RIG-I, Cause Atypical Singleton-Merten Syndrome. Am J Hum Genet, 96, 266-274. 3. Ferreira, C.R., Crow, Y.J., Gahl, W.A., Gardner, P.J., Goldbach-Mansky, R., Hur, S., de Jesus, A.A., Nehrebecky, M., Park, J.W. and Briggs, T.A. (2019) DDX58 and Classic Singleton-Merten Syndrome. J Clin Immunol, 39, 75-80. 4. Prasov, L., Bohnsack, B.L., El Husny, A.S., Tsoi, L.C., Guan, B., Kahlenberg, J.M., Almeida, E., Wang, H., Cowen, E.W., De Jesus, A.A. et al. (2021) DDX58(RIG-I)-related disease is associated with tissue-specific interferon pathway activation. J Med Genet. 5. Zheng, J., Wang, C., Chang, M.R., Devarkar, S.C., Schweibenz, B., Crynen, G.C., Garcia-Ordonez, R.D., Pascal, B.D., Novick, S.J., Patel, S.S. et al. (2018) HDX-MS reveals dysregulated checkpoints that compromise discrimination against self RNA during RIG-I mediated autoimmunity. Nat Commun, 9, 5366.
https://m.sciencenet.cn/blog-3423233-1339219.html
上一篇:《自然—结构与分子生物学》:张凯团队解析中央微管复合物结构并发现其主动调节机制
下一篇:《细胞》:清华大学柴继杰等首次证明2\',3\'-cAM/cGMP可由植物TIR蛋白产生并正向调控植物免疫反应