博文
减肥新靶标!北大邱义福团队发现褐色脂肪组织中存在一个“产热通道”
||
2022年8月16日,北京大学未来技术学院/北大-清华生命科学中心邱义福团队在Cell Metabolism发表题为“The mitochondrial calcium uniporter engages UCP1 to form a thermoporter that promotes thermogenesis”的研究论文【1】。
该研究首次报道在肾上腺素能刺激下,褐色脂肪细胞的MCU通过EMRE与UCP1互作,形成MCU-EMRE-UCP1复合物(命名为 “产热通道”,即“thermoporter”)来促进UCP1介导的解偶联呼吸和适应性产热。

肥胖已成为全球性的重大健康问题,在个体层面可以通过增加能量消耗来对抗肥胖。自2009年在成人中检测到代谢活跃的褐色/米色脂肪组织(BAT (brown adipose tissue) or beige fat)以来,科学家们一直在寻找增强褐色/米色脂肪产热从而增加能量消耗、抵抗肥胖的方法。褐色脂肪组织线粒体富含解偶联蛋白UCP1(uncoupling protein 1)。UCP1能够提高线粒体内膜对质子的电导性,从而消耗质子梯度,将氧化磷酸化与ATP合成解偶联,把底物氧化的能量转化为热能,以此介导褐色脂肪产热,从而帮助动物抵御低温、肥胖及相关代谢紊乱,是治疗肥胖及代谢疾病的重要靶标。线粒体钙离子单向转运体MCU(mitochondrial calcium uniporter)复合物是负责线粒体钙离子吸收的主要通道。该复合物包含孔道形成亚基MCU以及调节性亚基EMRE(essential MCU regulator)、MICU1/2(mitochondrial calcium uptake 1/2)等。其介导的钙离子吸收促进线粒体有氧呼吸,在三羧酸循环、电子转移、质子梯度累积和ATP合成中发挥关键作用。然而,MCU复合物介导的线粒体钙离子吸收是否调节褐色脂肪产热尚不清楚。
在这项最新研究中,作者发现,褐色脂肪特异性敲除Mcu或Emre的小鼠表现出寒冷不耐受、褐色脂肪产热能力减弱及UCP1介导的解偶联呼吸受损。作者分离纯化BAT 线粒体中的MCU复合物进行质谱鉴定,发现MCU复合物可能与UCP1存在互作。在BAT线粒体中利用免疫共沉淀、FLAG-Strep串联纯化和blue native PAGE等手段证实了褐色脂肪线粒体上MCU-EMRE-UCP1复合物的存在,并揭示该复合物的形成受肾上腺素能的诱导,且能被PKA急性调控。
接下来作者在BAT中定点注射AAV、表达adiponectin启动子驱动的串联蛋白EMRE-UCP1,促进了褐色脂肪线粒体上MCU-EMRE-UCP1复合物的组装。使用钙成像监测成熟褐色脂肪细胞中线粒体的钙离子吸收活性(即MCU活性)发现,去甲肾上腺素刺激可显著增加MCU-EMRE-UCP1复合物的组装并增强MCU活性。增强的线粒体钙离子吸收能够加速TCA循环、增加NADH产生,从而促进UCP1介导的解偶联呼吸和BAT产热。根据MCU-EMRE-UCP1复合物可增强线粒体钙离子吸收、促进解偶联呼吸和产热的特性,作者将其命名为thermoporter(thermogenic uniporter,产热通道)。此外,作者还发现MCU复合物中另外一个重要的调控亚基MICU1可通过抑制thermopoter的组装和功能负向调控产热。
最后,作者通过在ob/ob小鼠的BAT中增加thermopoter的组装来提高BAT产热能力,从而改善了ob/ob小鼠的寒冷不耐受。在BAT中增加thermopoter组装还可以帮助野生型小鼠有效对抗高脂饮食诱导的肥胖,提高小鼠的胰岛素敏感性和葡萄糖耐受性,改善小鼠的代谢失调。
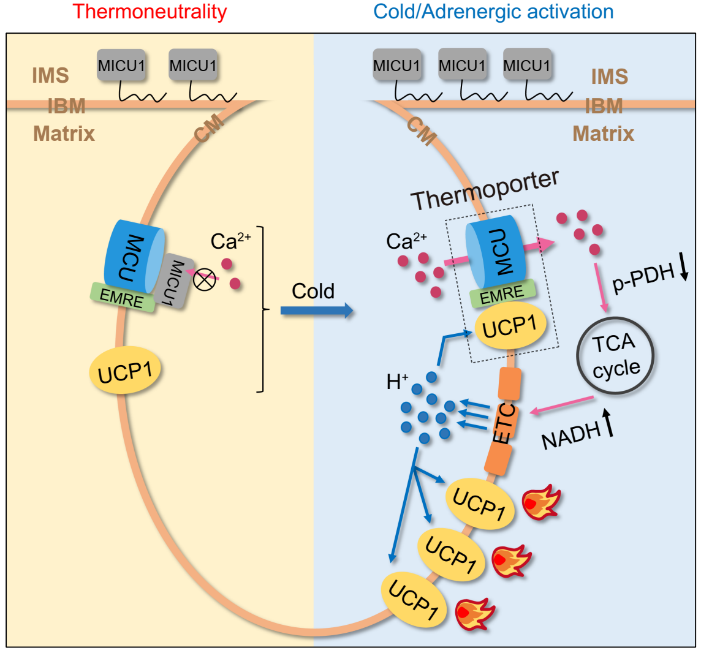
图一:“产热通道”促进UCP1介导的解偶联呼吸与适应性产热
总之,该研究发现褐色脂肪组织中存在MCU-EMRE-UCP1复合物这样一个“产热通道”(thermopoter),并揭示该通道具有响应寒冷和肾上腺素能刺激、增加线粒体钙离子吸收以促进解偶联呼吸和适应性产热的功能(图一)。“产热通道”的发现为肥胖的预防和治疗提供了新靶标。值得注意的是,极少部分的UCP1通过与MCU-EMRE互作形成“产热通道”,却极大地促进了所有UCP1的解偶联呼吸,表明UCP1在解偶联之外还发挥信号分子的作用。
北京大学未来技术学院分子医学研究所博士毕业生薛凯丽为文章第一作者,邱义福研究员为通讯作者。邱义福实验室吴冬梅博士和博士生王玉双也对本研究做出了重要贡献。本研究得到北京大学肖瑞平教授、程和平院士,清华大学王一国教授,中科院动物所金万洙研究员的大力支持和帮助。
北京大学未来技术学院/北大-清华生命科学中心邱义福实验室长期从事代谢应激生物学研究,围绕肥胖及相关代谢疾病,从三个方面开展研究:能量代谢的免疫调控、褐色/米色脂肪的发育与功能、脂肪组织的动态重塑。除了上述“产热通道”的发现,我们近期还阐明了巨噬细胞调节肥胖及代谢炎症的一条新通路【2】。
现因发展需要诚聘博士后,从事代谢应激生物学研究。邱义福研究员通过北大未来技术学院及北大-清华生命科学中心招生,欢迎研究生申请。有意者请将个人简历等材料发送至:yifu.qiu@pku.edu.cn。
相关论文信息:
https://doi.org/10.1016/j.cmet.2022.07.011
参考文献
1.Xue K, Wu D, Wang Y, Zhao Y, Shen H, Yao J, Huang X, Li X, Zhou Z, Wang Z, Qiu Y*. (2022). The mitochondrial calcium uniporter engages UCP1 to form a thermoporter that promotes thermogenesis. Cell Metabolism, https://doi.org/10.1016/j.cmet.2022.07.011.
2.Yao J, Wu D, Zhang C, Yan T, Zhao Y, Shen H, Xue K, Huang X, Wang Z, Qiu Y*. (2021). Macrophage IRX3 promotes diet-induced obesity and metabolic inflammation. Nature Immunology, 22, 1268-1279.
https://m.sciencenet.cn/blog-3423233-1351595.html
上一篇:《自然》:耶鲁大学樊荣团队发布空间分辨的染色质可及性测序新技术
下一篇:《细胞》:郭红卫/柴继杰合作团队揭示植物感知胞外pH的机制