博文
“∑(μi·dni)”的热力学内涵
|
“∑(μi·dni)”是平衡态热力学教学中出现频率较高的一物理量. 本文拟结合具体的热力学过程,介绍“∑(μi·dni)”的热力学内涵.
“∑(μi·dni)”是典型的热力学过程量,不同的热力学过程,其含义有差别.
1. 气体的pVT变化
例1. 298.15K、100kPa下1摩尔氮气,恒温条件下膨胀至80kPa,计算该过程的ΔG.
解:对应的热力学过程参见如下图1.
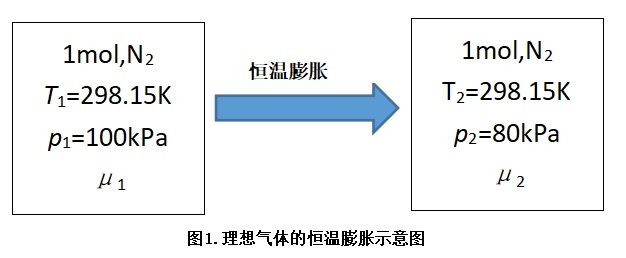
由热力学基本方程可得[1]:dG=-S·dT+V·dp+δW' (1)
依题:该过程恒温及有效功为0,即:dT=0, δW' =0.
将上述条件代入式(1)可得:dG=V·dp (2)
另:ΔG=∫∑(μi·dni)=μ2×+μ1×
=μ2×1mol-μ1×1mol=μ2-μ1 (3)
结合式(2)与(3)可得:
ΔG=μ2-μ1 =∫(n·RT/p)·dp (4)
整理式(4)可得:ΔG=μ2-μ1 =n·RT·ln(p2/p1) (5)
将已知条件代入式(5)可得:
ΔG=μ2-μ1 =1mol×8.315J·mol-1·K-1×298.15K×ln(100kPa/80kPa)
=553.20J
由上可得:理想气体的pVT变化中,∑(μi·dni)的积分结果,等于系统终态的吉布斯能减去系统始态的吉布斯能,即: ΔG=G2-G1=∫∑(μi·dni)=μ2-μ1,与热力学过程是否恒压无关.
2. 相变
例2. 298.15K、100kPa下1摩尔液态水挥发为水蒸气,计算该过程的ΔrGθm.
解:对应的热力学过程参见如下图2.
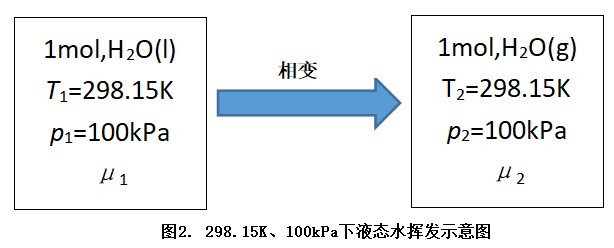
由热力学基本方程可得:dG=-S·dT+V·dp+δW' (1)
依题:该过程恒温、恒压及环境不提供有效功,即:dT=0,dp=0, δWe'=0*.
*备注:δW'=δWe'+δWs' (6)
式(6)中δWe'代表环境提供系统的有效功;δWs'代表系统自身产生的有效功.
依题δWe'=0, δW'=δWs'
将上述条件代入式(1)可得:dG=δW'=δWs' (7)
ΔrGθm=∫∑(μi·dni)=μ2×+μ1×
=μ2×1mol-μ1×1mol=μ2-μ1 (8)
另由热力学基本原理可得[2]:
ΔrGθm=∑(νi·ΔfGθm,i)=ΔfGθm(H2O,g)-ΔfGθm(H2O,l)
=-228.572kJ·mol-1-(-237.129)kJ·mol-1
=8.557kJ·mol-1>0
计算结果表明,298.15K、100kPa下1摩尔液态水挥发为水蒸气为非自发过程.
由上可得:相变中,∑(μi·dni)的积分结果,等于系统终态的吉布斯能减去系统始态的吉布斯能,即:∫∑(μi·dni)=G2-G1.
3. 化学反应
例3. 298.15K、100kPa下化学反应N2(g)+3H2(g)=2NH3(g),计算该过程的ΔrGθm.
解:对应的热力学过程参见如下图3.
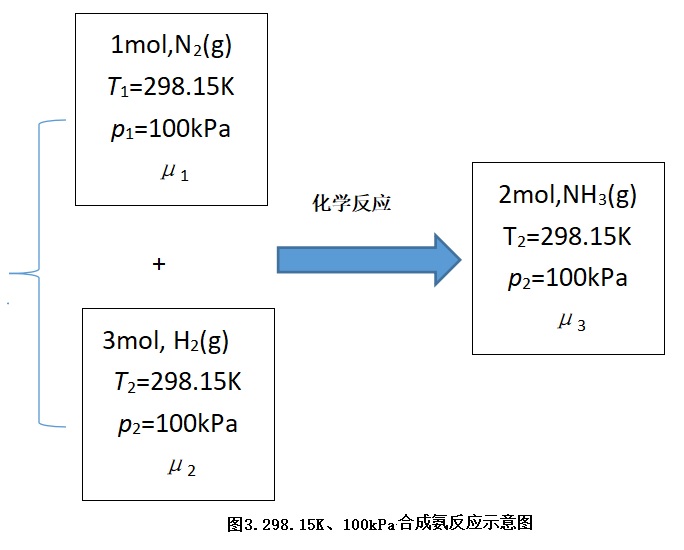
由热力学基本方程可得:dG=-S·dT+V·dp+δW' (1)
依题:该过程恒温、恒压及环境不提供有效功,即:dT=0,dp=0, δWe'=0.
将上述条件代入式(1)可得:dG=δW'=δWs' (9)
ΔrGθm=∫∑(μi·dni)=μ3×+μ1×
+μ2×
=μ3×2mol-μ1×1mol-μ2×3mol=2μ3-3μ2-μ1 (10)
另由热力学基本原理可得:
ΔrGθm=∑(νi·ΔfGθm,i)=2ΔfGθm(NH3,g)-3ΔfGθm(H2,g)-ΔfGθm(N2,g)
=2mol×(-16.45)kJ·mol-1
=-32.90kJ·mol-1<0
计算结果表明,298.15K、100kPa下合成氨的反应为自发过程.
由上可得:合成氨的化学反应中,∑(μi·dni)的积分结果,等于系统终态的吉布斯能减去系统始态的吉布斯能,即:∫∑(μi·dni)=G2-G1.
4.结论
⑴∑(μi·dni)的积分结果,等于系统终态的吉布斯能减去系统始态的吉布斯能
⑵ 由气体pVT变化讨论可知:dG=∑(μi·dni)=-S·dT+V·dp+δW' 较dG=-S·dT+V·dp+∑(μi·dni)更合理.
参考文献
[1]余高奇. 热力学第一定律研究.http://blog.sciencenet.cn/u/yugaoqi666 .科学网博客, 2021,8.
[2] Lide D R. CRC Handbook of Chemistry and Physics. 89th ed, Chemical Co, 2008,17:2688.
https://m.sciencenet.cn/blog-3474471-1354526.html
上一篇:溶剂压(Π)与大气压(p)应用实例
下一篇:热力学状态函数全微分的逻辑性探讨