博文
混合过程的熵变计算探究(Ⅱ)
|
本文拟在“混合过程的熵变计算探究”的基础上[1],结合具体实例,进一步探讨理想液态混合物混合过程
dG=∑μidni=-SdT+Vdp+δW' 的积分式,并给出 现象的一种可能解释.
现象的一种可能解释.
[例1] 25℃下,由各为0.5mol的纯溶剂A与B混合形成理想液态混合物,试计算该混合过程ΔmixG与ΔmixS .
1. dG积分式的探讨
dG=∑μidni=-SdT+Vdp+δW' (1)
式(1)是理想液态混合物混合过程最重要的热力学基本方程式之一.
理想液态混合物混合条件为:①恒温(或dT=0);②δW'=0(因没有化学反应或相变发生).
将上述两条件代入式(1)可得:
dG=∑μidni=Vdp (2)
另理想液态混合物中任一组分B的化学势可表示为: μB= μB*+RT·lnxB (3)
式(2)积分,并结合式(3)可得:
ΔmixG=G终态-G始态
=[0.5mol×(μA*+RT·lnxA)+0.5mol×(μB*+RT·lnxB)]-(0.5mol×μA*+0.5mol×μB*)
=0.5mol×RT·lnxA+0.5mol×RT·lnxB (4)
依例1,xA=xB=0.5mol/(0.5mol+0.5mol)=0.5 (5)
将式(5)代入式(4)可得:
ΔmixG=0.5mol×8.314J·K-1·mol-1×298.15K×ln0.5+0.5mol×8.314J·K-1·mol-1×298.15K×ln0.5
= -1.7182kJ·mol-1 (6)
另:![]() (7)
(7)
将式(6)结果代入式(7)可得:
![]() (8)
(8)
整理式(8)可得:ΔmixS= 5.7628J·K-1·mol-1
2. 溶剂压与Vdp的积分式探讨
为解释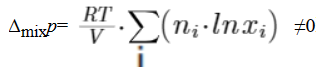 现象,特引入溶剂压(Π)及溶剂压常数(k).
现象,特引入溶剂压(Π)及溶剂压常数(k).
2.1 溶剂压(Π)
同气体分子不停碰撞容器壁并产生压强一样,溶剂分子也产生溶剂压(Π).
溶剂压定义参见如下式(9).
Π=nRT/ V (9)
式(9)中,Π代表溶剂压,单位为Pa;n表示溶剂的物质的量,单位为mol;R表示摩尔理想溶剂常数,
R=8.314J·K-1·mol-1;T为体系温度,单位为K;V代表溶剂总体积,单位为m3.
另理想液态混合物中任一i组分的溶剂压:Πi=ni·RT/ V (10)

不同溶剂混合时,溶剂压将发生作用,需消耗能量;可表示为:
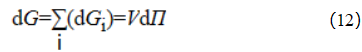
由式(9)可得:![]()
将式(13)代入式(12),并积分可得:

由式(14)可得:ΔmixGi=ni·RT ·ln(Π终态/Π始态) (15)
2.2 溶剂压常数(k)
通常情况下,某溶剂(i)的溶剂压(Πi)与理想液态混合物中该溶剂的物质的量分数(xi)成正比;参
见如下式(16): Πi=ki·xi (16)
式(16)中ki称溶剂压常数,ki与温度及溶剂i的性质有关,与溶剂体积及理想液态混合物中其它溶剂无
关. ki的单位为Pa.
另需指出:溶剂压常数(ki)也可解读为一定温度时,某i纯溶剂所拥有的溶剂压.
则:Π终态,i=ki·xi (17)
Π始态,i=ki (18)
将式(17)及(18)代入式(14)可得:
ΔmixG=∑(ΔmixGi)=RT·∑(ni ·lnxi) (19)
由式(19)可得:ΔmixGi=ni ·RT·lnxi (20)
3.结论
⑴Π=nRT/ V ,Πi=ni·RT/ V;
⑵Πi=ki·xi ;
⑶ ΔmixG=∑(ΔmixGi),ΔmixGi=ni ·RT·lnxi .
参考文献
[1]余高奇.混合过程的熵变计算探究.http://blog.sciencenet.cn/u/yugaoqi666. 科学网博客, 2023,2.
https://m.sciencenet.cn/blog-3474471-1374723.html
上一篇:混合过程的熵变计算探究
下一篇:相平衡教学中常见几个问题的解答