博文
生物3D打印厘米级血管化组织
||
生物3D打印构建厘米级血管化组织
大尺寸组织的构建需要良好的血供系统,然而,厘米级的大尺寸组织的生物3D打印相比小尺度组织具有诸多苛刻要求,主要有以下两方面:
l 物质在大尺度结构内扩散:水凝胶材料自发形成的孔隙主要分布在微米尺度上。因此,营养物质、氧气和细胞代谢物在厘米级组织中的分布通常具有梯度。大尺寸组织内的细胞由于营养、氧气的缺乏难以存活,且细胞代谢产物不能顺利排出。因此,大厘米级组织内需要构建更大、更丰富的营养通道网络;
l 血管化网络构建:在实际的生物体中,不同尺度的血管网络分布在组织中,为周围的细胞提供必要的血液供应。因此,为了更贴近生物体内的组织,除了应在厘米级组织中负载组织主体细胞,内部还应构建复杂的3D血管网络。
明胶微球是具有温敏特性的特殊微结构,其可在低温条件下维持弹性体形态,而在高温条件下可融化为液体。基于明胶微球的温敏特性,浙江大学贺永教授团队(EFL团队),提出了可控孔隙的大尺寸组织构建思路:通过明胶微球实现打印组织内的有序孔隙结构,将混合组织主体细胞及血管内皮生长因子(VEGF)的GelMA水凝胶预聚液作为墨水的主体组分,将负载人血管内皮细胞的明胶微球作为墨水的辅助组分,实现了厘米级多孔血管化大组织的打印。
本方法有如下特点:
n 通过挤出式生物3D打印机打印将其打印为厘米级结构,沉积结构通过405nm蓝光交联GelMA预聚液;
n 交联结构在37℃培养箱内培养后,内部的明胶微球将融化为液态并逐渐扩散至GelMA结构外部,形成球形孔隙营养通道,同时释放负载的内皮细胞;
n 内皮细胞在孔隙内壁贴附,并在外部GelMA内的VEGF因子与组织细胞的共同作用下逐渐形成三维出芽,构成大尺寸结构内的血管网络(图1)。
相关研究“Thermo-sensitive Sacrificial Microsphere-based Bioink for Centimeter-scale Tissue with Angiogenesis”发表在International Journal of Bioprinting期刊上,浙江大学机械工程学院贺永教授、浙江省人民医院王吉医师为共同通讯作者,谢明君博士、孙元博士为该论文的共同第一作者。

图1. 温敏牺牲型微球基生物墨水的制备及多孔厘米级血管化大组织的形成原理
为了探究明胶微球的电喷制备工艺,研究人员通过改变电喷电压探索了明胶微球的尺寸变化规律(图2),以此可按需制备不同直径的明胶微球以在结构内形成不同的营养通道。此外,研究人员测试了不同的明胶微球组成的“温敏牺牲型”墨水的流变性,对明胶微球的牺牲特性和墨水可打印性进行了验证(图3)。
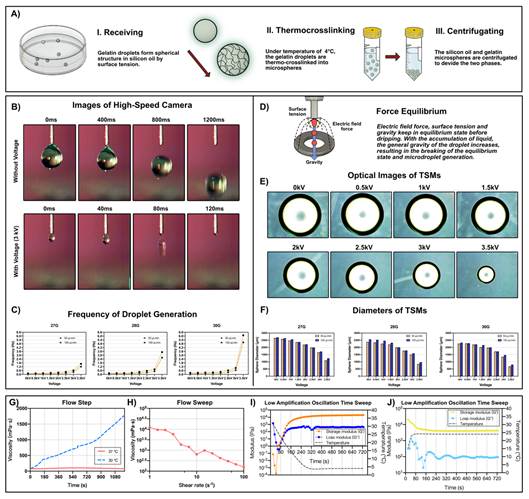
图2. 温敏牺牲型微球的电喷工艺研究

图3. 温敏牺牲型微球基生物墨水的流变性能
为了获得具有不同营养通道分布的厘米级结构,不同直径和不同体积配比的明胶微球被添加至GelMA预聚液中并固化成型(图4)。为了便于在共聚焦荧光显微镜下观察营养通道的形态,在 GelMA 预聚液中添加了少许荧光GFP-GelMA。随着明胶微球体积比例的增加,营养通道的数量增加,分布更加均匀。通过混合不同直径的明胶微球,可以形成不同大小的营养通道。随着明胶微球直径的降低,营养通道的分布变得更加均匀。此外,墨水的可打印性得到了证实,通过该墨水体系可以构建不同的二维图案及三维结构(图5)。
图4. 厘米级结构内按需构建营养通道

图5. 温敏牺牲型微球基生物墨水的挤出可打印性
相比于实体GelMA结构,由“温敏牺牲型”墨水构建的多孔大组织内人乳腺癌细胞可正常存活,且可在结构内实现三维伸展(图6)。由明胶微球释放的内皮细胞可成功贴附于球形孔隙内壁,并在GelMA结构内的VEGF诱导下实现三维出芽(图7、图8)。

图6. 多孔厘米级结构内人乳腺癌细胞的生长情况

图7. 多孔厘米级结构内的HUVECs出芽

图8. 多孔厘米级结构内HUVECs相关蛋白表达情况
将人乳腺癌细胞与内皮细胞同时负载于该墨水体系中,经过7天的培养,可以发现内皮细胞向人乳腺癌细胞区域形成更长的出芽,并且在肿瘤组织中形成了更多的血管分支。经过12天的培养,来自不同营养通道的内皮细胞出芽开始相互汇合。由于负载的乳腺癌细胞分泌了VEGF,三维血管网络生成现象更加明显,三维血管网络变得更加复杂(图9)。结果表明,基于提出的“温敏牺牲型”墨水可成功实现厘米级血管化乳腺肿瘤组织的体外打印,证明了其在生物医学领域中的应用潜力。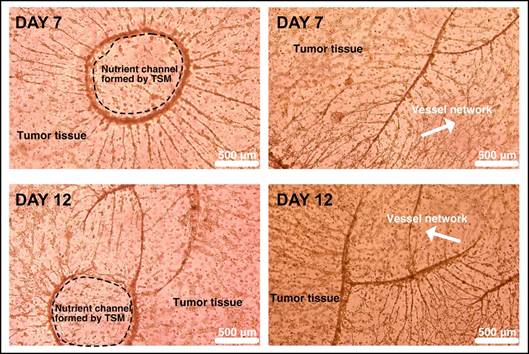
图9. 厘米级血管化乳乳腺癌组织打印
致谢:本研究受到了国家重点研发变革性专项(2018YFA0703000)、国家自然科学基金联合基金重点(U1909218)及国家自然科学基金创新群体(T2121004)项目支持。
全文链接:https://ijb.whioce.com/index.php/int-j-bioprinting/article/view/599
https://m.sciencenet.cn/blog-2159320-1352623.html
上一篇:GelMA水凝胶实现树突状免疫细胞的高质量培养
下一篇:生物水凝胶微结构快速制造方法助力心肌细胞定向可控生长