博文
诺奖--化学渗透耦合理论
||||
本博文和前文“诺奖—ATP的生物合成”实际上是相同的题目但是内容上更是着重于现代热力学理论方面。一般来说,物理口的老师不太熟悉化学反应,有的更害怕复杂的生物化学反应。其实这样的顾虑是多余的,只要把“生物化学”或“化学”的“反应”看成一个从初态A(二磷酸腺苷ADP+无机磷酸Pi)到终态B(三磷酸腺苷ATP)的“过程”就行。为什么叫“耦合”,就是同时还有一个从另一初态C(高浓度的质子)到另一终态D(高浓度的质子)的“渗透”过程,而且前者是需要能量(或称自由能)的非自发过程,后者是可以提供能量的自发过程,仅此而已。前者不能单独自发进行,通过和后者的耦合(或称克劳修斯的“补偿”)于是就可以进行了。早在1865年克劳修斯就说:
按我已经给出的第二基本原理形式, 可以断言所有发生在自然界的转变可以沿着它们自己确定的方向, 我设定为正, 没有补偿地自己进行; 但是反过来说, 它们要按负方向进行就只可能在同时发生的正转变的补偿下进行.
请注意:克劳修斯的的正方向的转变“没有补偿地自己进行”就是我在上面所说的自发反应;而克劳修斯的负方向的转变“就只可能在同时发生的正转变的补偿下进行”就是我在上面所说的非自发反应只可能在同时发生的自发反应的耦合下进行。当然克劳修斯在当时并没有把“补偿”的数学表达式写出来。
第一个提出热力学耦合或“补偿”数学表达式的人不是物理学家而是一位生物化学家勃欧克(Dean Burk). 在1931年他是直接根据热力学第二定律提出热力学耦合的数学表达式[DF1 > 0, DF2 < 0 & DF £ 0],即现在的等温等压形式[(DG1)T,p > 0, (DG2)T,p < 0 & (DG)T,p £ 0]。请注意这时已经包含了等式和不等式两部分。后来又逐步完善成普适的热力学耦合数学表达式[diS1 < 0, diS2 > 0 & diS ³ 0]。注意:热力学耦合数学表达式就是现代热力学第二定律的数学表达式,也同样包含了等式和不等式两部分。一定要注意:任何用“微观机理”来否定热力学的宏观普适严谨结论的尝试都是不可能成功的,因为据我所知这在历史上没有成功先例的。
为了方便和帮助人们的理解,生物化学家很早就用两个相互交叉的箭头来表示生物化学中的大量热力学耦合现象。两个箭头的交叉点就是表示有能量的传递。例如,对化学渗透耦合理论可以简单地表示为图1(a),对更多的耦合反应就可以表示为图1(b)。这两种表示方法都表示两个不可逆过程之间的热力学耦合。
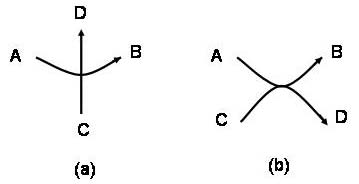
图 1
热力学第二定律对热力学耦合的唯一限制就是等温等压下由初态A到终态“过程”中得到的吉布斯自由能不可能大于从另一初态C到另一终态D “过程”所提供的吉布斯自由能。于是就得到整个体系的吉布斯自由能变化等于零和小于零两部分,即[(DG1)T,p > 0, (DG2)T,p < 0 & (DG)T,p £ 0] 成立。或者用熵产生来说,任何体系中负的过程熵产生不可能大于正的过程熵产生。于是就得到体系的熵产生等于零和大于零两部分,即[diS1 < 0, diS2 > 0 & diS ³ 0] 成立。
最后还可以强调一下,热力学耦合的数学表达式中等式和不等式都没有也不可能违反热力学第二定律,因为这样的数学表达式同时就可以被称为是现代热力学第二定律的数学表达式。
https://m.sciencenet.cn/blog-307912-308010.html
上一篇:严谨要求 统一明示 深层讨论
下一篇:严格区分两种不同“百分之百”