博文
《自然—生物医学工程》:新加坡南洋理工大学浦侃裔团队首次报道声致余辉分子探针用于肿瘤诊疗
||
2022年12月23日,新加坡南洋理工大学浦侃裔教授团队在《自然—生物医学工程》发表论文,首次报道了超声激活的、基于有机材料的活体余辉探针(SNAP)用于深部组织声致余辉成像。
SNAP主要负载了两类探针分子:声敏剂和余辉底物。前者可在超声刺激下产生单线态氧,后者则可与单线态氧反应生成高化学能的dioxetane中间体。中间体的化学能以光子形式缓慢释放,因而超声停止后可产生余辉发光。得益于超声的组织穿透力,余辉探针信号通过4厘米组织后仍能被检测到,成像深度为荧光成像的两倍以上。

分子影像学利用分子探针对细胞和亚细胞结构和功能进行定性定量研究,在生理监测、疾病诊断、药物筛选和预后评估等生命科学重大领域有着重要应用。余辉成像是一种利用有机(如半导体聚合物)或无机(如稀土掺杂纳米粒)材料作为“光学电池”将激发光的光能暂时存储、而在光照射停止后缓慢地释放光子的成像模式。相比于依赖实时激发光的荧光成像,余辉成像具有更高的信噪比和灵敏度。同时,基于对探针结构的灵活改造,余辉发光具有可调谐可见光区至近红外区发射、可重复激活以及长寿命的优点。
早在2017年,浦侃裔教授团队首次报道了以有机材料为主的光致余辉探针及其成像机制,并将其用于活体肝脏损伤的早期检测(Nature Biotechnology, 2017, 35, 1102–1110)。此后,多种基于有机材料的光致余辉探针被相继研发并广泛用于肿瘤精准诊断、治疗药物监测以及术中影像指导等。然而,由于生物组织对激发光的散射和吸收,激发光难以穿透到深部组织,光致余辉在深部组织成像中的应用受到较大限制。
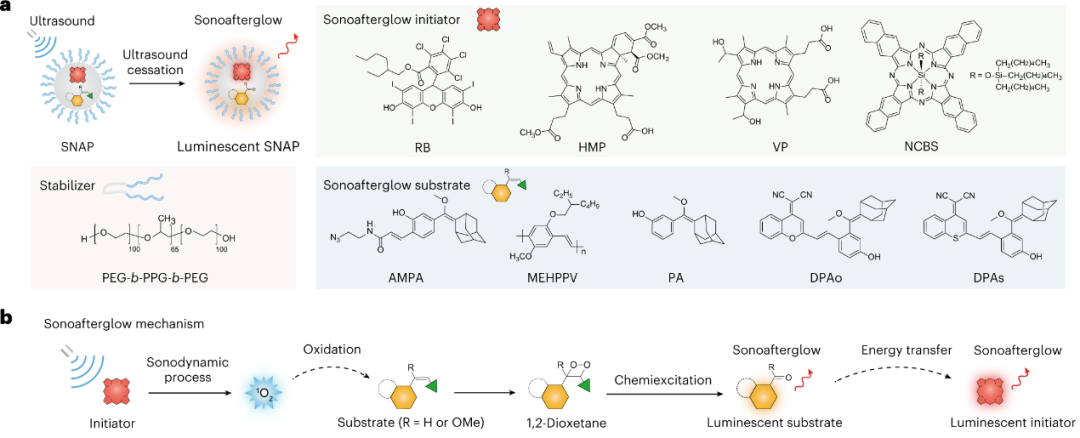
图1. 声致余辉探针的构建(a)和成像机制(b)
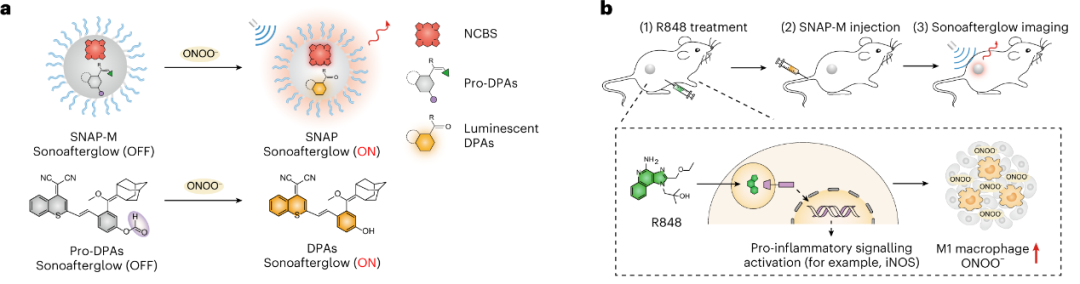
图2. 微环境响应性声致余辉探针构建(a)和小鼠肿瘤炎性环境成像模式图(b)
应用一: 生物标志物的检测。该研究团队进一步制备了可激活探针(SNAP-M)用于肿瘤炎性微环境的实时监测。基于余辉底物分子对微环境中的M1型巨噬细胞代谢产物peroxynitrite(ONOO-)的响应,M-SNAP介导的声致余辉能够有效反映微环境炎症因子水平,对评估肿瘤预后具有显著的指导意义。
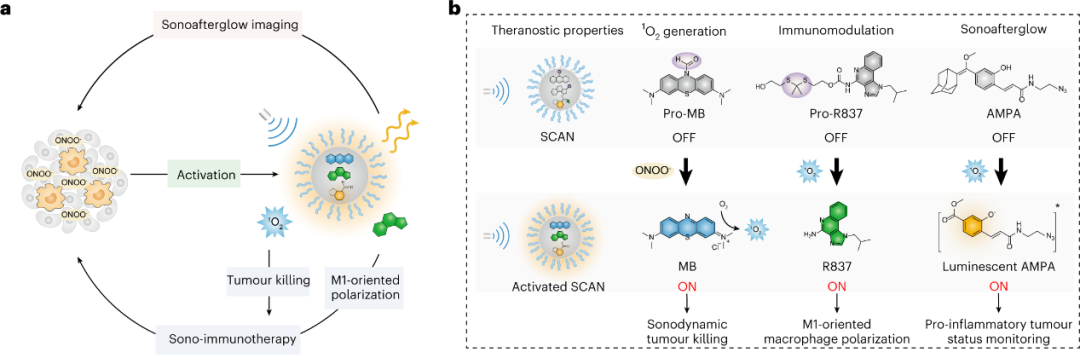
图3. 微环境响应性声致余辉探针用于肿瘤诊疗(a及其机制(b)
应用二: 声致余辉介导肿瘤治疗。该研究团队进一步设计了ONOO-响应性可激活探针(SCAN),其负载了余辉底物、ONOO-响应性声敏剂和单线态氧激活的免疫治疗前药。ONOO-激活后的声敏剂分子可在超声刺激下产生单线态氧,不仅介导声动力肿瘤治疗,还能激活前药以诱导巨噬细胞M1型转化,发挥免疫治疗作用。同时,由于 ONOO-水平与余辉信号具有显著相关性,声致余辉得以反映肿瘤内M1巨噬细胞水平及免疫治疗效果。综上,SCAN实现了一体化肿瘤诊疗。
新加坡南洋理工大学浦侃裔教授为该论文的通讯作者,博士生徐程、黄景胜为共同第一作者。
该项目得到Singapore National Research Foundation和 Singapore Ministry of Education 等项目的资助。
相关论文信息:
https://doi.org/10.1038/s41551-022-00978-z
https://m.sciencenet.cn/blog-3423233-1369790.html
上一篇:清华大学郗乔然/吝易课题组合作揭示PML核体招募TRIM33在小鼠胚胎干细胞中调控基因转录的新机制
下一篇:《自然—生物技术》:北京大学李毓龙实验室开发新型催产素荧光探针揭秘神经肽的时空动态调控