博文
代谢学人--Journal of Hepatology:促癌祸手-pIgR小囊泡
||
撰文 | 徐梓禾 于柳 陈俊桐 邱瑾 徐鑫铭
编辑 | 孟美瑶
校对 | 陈俊桐

背景介绍
世界卫生组织估计,2030年将有100多万患者死于肝癌,其中大部分会是肝细胞癌(HCC)。肝细胞癌(HCC)占原发性肝癌中的大多数,目前是全球第四大癌症死亡的病因。肝癌通常在晚期才被诊断出来,并且晚期HCC的治疗选择也十分受限,无法对肿瘤进行根治性消除。因此,阐明HCC侵袭性属性的潜在机制对于患者的诊断和治疗至关重要。
越来越多的证据表明,除了通过细胞间直接接触和细胞分泌型可溶性因子介导之外,细胞间交流还可由细胞外囊泡(EVs)来介导。EVs是生物膜衍生的纳米级囊泡,能将供体细胞分泌的生物活性分子(可包含脂质、核酸和蛋白质等)转移到受体细胞中,来实现细胞/组织器官间的代谢交流。肿瘤微环境是支持癌细胞生长、生存和转移的复合环境。显然,癌细胞分泌的EVs是连接肿瘤细胞与其局部和远处微环境的关键信使,可协调多种系统病理的生理过程以促进癌症发展。尽管EVs在癌症发展中有多种作用,但EVs与肿瘤干细胞(CSCs)相关的作用仍不确定,且EVs在肝脏CSCs中的功能也鲜有报道。有研究报道,在化学诱导的HCC大鼠模型中,肝脏CSCs分泌的EVs增强了肿瘤的生长和转移。此外,来自CD90+肝癌细胞的EVs能够调节内皮细胞以促进HCC中的血管生成。因此,CSC和EVs在HCC中的重要影响提示了理解EVs和肝脏CSC之间联系对于疾病治疗的重要性。
聚合免疫球蛋白受体(pIgR)在粘膜上皮细胞中广泛表达,并调节二聚体IgA和五聚体IgM的细胞转运,二者都是抵抗初始感染的一线抗体。在病毒或细菌感染时,促炎细胞因子上调pIgR的表达,从而架起先天免疫和适应性免疫之间的桥梁。已有新发现揭示了pIgR在癌组织中的异常表达。然而,pIgR在肿瘤细胞中的功能仍不确定。在本文中,作者就首次证实了pIgR是HCC患者循环EVs产生致癌作用的关键分子。

1、肝癌患者的循环EVs中pIgR水平升高。
2、EV-pIgR促进受体肝癌细胞的癌症干细胞和癌症表型。
3、EV-pIgR通过激活PDK1/Akt/GSK3β/β-连环蛋白信号通路促进肝癌细胞的侵袭性。
4、索拉非尼和抗pIgR抗体的联合治疗可抑制小鼠体内患者肿瘤组织来源移植瘤的生长。
研究结果
来自HCC细胞系的EVs在增强HCC侵袭性方面发挥着关键作用,但其对HCC患者影响的生理相关性仍不明确。收集健康个体(Normal-EVs)和慢性HBV(乙型肝炎病毒)感染的肝硬化患者(Cirrhosis-EVs)、早期HCC(E–HCC–EVs)或晚期HCC(L–HCC–EVs)患者的循环EVs进行功能分析。根据细胞外囊泡研究最低指导要求(MISEV),对EVs的标志蛋白表达、大小和形态进行了验证(附图1A-C)。值得注意的是,与其他血清来源的EVs相比,从晚期HCC患者获得的EVs数量最多(附图1D)。
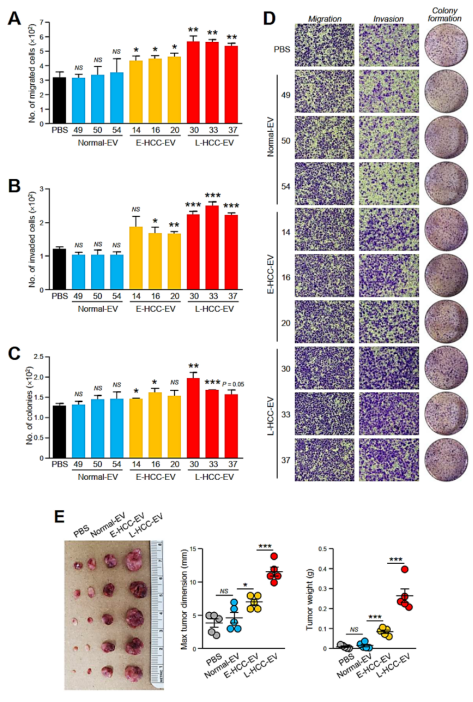
与Normal-EVs相比,来源于HCC患者的EVs增加了Huh7和PLC/PRF/5细胞的增殖速率和细胞活力(附图2A-D)。与Normal-EVs、Cirrhosis-EVs和E-HCC-EVs相比,L-HCC-EVs能够促进细胞迁移、侵袭和克隆形成(图1A-B)进而在促进肿瘤发展方面表现出最高的效力(附图2E)。在原位肝移植小鼠模型中,反复向小鼠体内注射L–HCC–EVs可增强肝脏肿瘤形成和肿瘤肺转移(图1C-E)。在同时注射EVs和p53-/-&Myc转导-肝母细胞的小鼠模型中,L–HCC–EVs在促进肿瘤转移方面也出现了与上述相一致的结果(图1F-H)。同时,L–HCC–EVs被证实可降低人脐静脉内皮细胞中紧密连接蛋白VE钙粘蛋白的表达(附图3),并增强小鼠的内皮通透性(图1I)。这些发现表明,肝脏肿瘤细胞的迁移可能归因于L–HCC–EVs诱导的肺血管渗漏,从而促进了肿瘤细胞在肺部的外渗和定植。
拓展阅读
Hepatoblasts(肝母细胞)
肝母细胞又称成肝细胞,是肝细胞和胆道上皮细胞的常见祖细胞,具有双向分化潜能,保留了干细胞的特性,有自我更新能力。
肝脏起源于腹侧前肠内胚层细胞(一种多潜能干细胞)。在小鼠中,前肠的原始上皮细胞接触心肌中胚层后快速增殖,形成肝原基。大约1d后,原始上皮细胞侵入原始横膈,继续分化为幼稚肝脏上皮细胞,这些细胞先表达 AFP (甲胎蛋白)然后是ALb(白蛋白)。幼稚肝脏上皮细胞很快成熟,并进一步分化为肝细胞或胆管上皮细胞,因为此期的肝脏上皮细胞其具有向这两种肝实质细胞双向分化的潜能,所以又称肝母细胞,小鼠胚胎肝母细胞分离自胚胎肝组织,用于进行肝脏代谢和肿瘤等方面的研究。
本文中,作者通过利用p53-/-&Myc转导小鼠的肝母细胞的实验性转移试验来构建肝癌细胞的模型,p53是抑癌基因(主要功能:抑制癌变、修复缺陷),Myc是原癌基因(主要功能:促进细胞增殖、恶性转化),在抑癌基因p53缺失情况下,作者利用HBV实现在肝母细胞中特异性的高表达Myc基因,构建HCC小鼠模型,来分析L–HCC–EVs对肝脏肿瘤的影响。
参考文献:

图1. HCC患者的循环EVs促进HCC细胞侵袭性
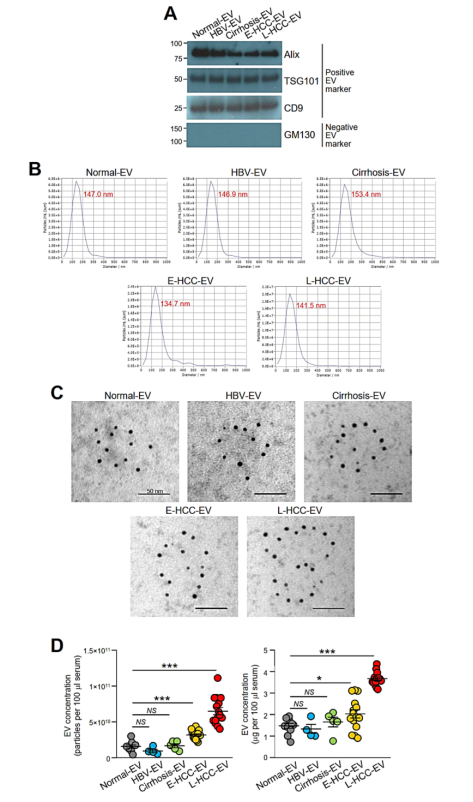
附图1. 从对照个体和患者血清中提取EVs的特征
附图2. 肝癌患者的循环EVs促进肝癌细胞的集落形成、迁移和侵袭
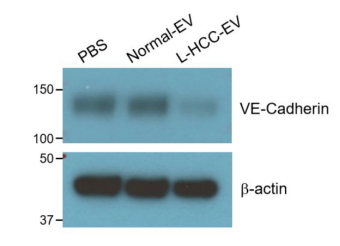
附图3. 晚期肝癌患者循环EVs降低内皮细胞紧密连接蛋白表达
2.HCC患者来源的EVs促进HCC细胞的肿瘤干细胞(CSC)特性
除了调节肿瘤细胞的癌症表型外,L–HCC–EVs还增加了HCC细胞的癌症干细胞特性。与Normal-EVs相比,用L–HCC–EVs处理的HCC细胞在肿瘤球形成实验中显示出更强的成球能力(图2A),并且CSC标记物CD90和CD133的表达量显著增强(图2B)。L–HCC–EVs还增加了Huh7(人肝癌细胞系)细胞中CD24、CD47和EpCAM的表达,但并不增加PLC/PRF/5(人肝癌亚力山大细胞)细胞中的表达,提示L–HCC–EVs能够促进部分而非全部HCC细胞系的CSC特性。(附图4)。此外,L–HCC–EVs降低了细胞对索拉非尼(一种新型多靶向性的治疗肿瘤的口服药物)的敏感性(图2C)。使用有限稀释法来评估不同EVs对NOD/SCID小鼠的影响,通过分析信号,详细监测了HCC细胞对于不同EVs的反应频率与程度。结果表明,与PBS或Normal-EVs处理的细胞相比,用L–HCC–EVs处理的HCC细胞表现出其成瘤能力显著增强,肿瘤发生率增加,肿瘤潜伏期缩短、肿瘤起始细胞(一小部分具有长期致瘤能力的肿瘤细胞,又称为肿瘤干细胞)数目增加等表型(附表2)。经L–HCC–EVs处理的肿瘤细胞移植到继发受体小鼠(小编注:多代肿瘤移植实验。正确使用异种移植检测来识别和表征人类肿瘤中的肿瘤干细胞的关键要素是进行严格的有限稀释法和多代肿瘤移植。在有限稀释法中,肿瘤干细胞频率是通过移植越来越稀释的单细胞制剂来测量的。在针对每个细胞剂量评估肿瘤再生之后,可以估计存在于给定细胞群中可以再生异种移植肿瘤的癌细胞的频率)中,可进一步提高肝脏肿瘤细胞的自我更新能力(图2D)。在初次和二次(小编注:实验先使肿瘤组织在小鼠体内生长形成第一代移植瘤,待其生长到一定大小时,取出该移植瘤组织并在无菌操作条件下移植到新一批免疫缺陷鼠的皮下,形成第二代移植瘤)都植入后,L–HCC–EV处理的细胞的无瘤生存率明显低于PBS或Normal-EVs处理的细胞(图2E)。
拓展阅读
肿瘤成球实验
肿瘤球(tumorsphere)是肿瘤细胞在无血清的培养条件下经表皮生长因子(epidermal growth factor EGF)和碱性成纤维细胞生长因子(basic fibroblast growth factor FGF)等多种细胞生长因子诱导形成的悬浮生长的细胞团块。肿瘤干细胞(CSC)是一群既具有自我更新能力又具有较强的侵袭迁移的细胞,对肿瘤的存活、增殖、转移及复发有着重要作用。肿瘤成球实验的步骤是将肿瘤组织经酶消化和机械分离成为单细胞悬液后,接种在含无血清培养基的超低黏附细胞培养板或培养瓶中(注意不要贴壁),培养过程中可以适当补充生长因子,如EGF, FGF。在此条件下,肿瘤干细胞将缓慢增殖,最终单细胞可形成非粘附肿瘤球。
肿瘤细胞的成球实验(成球大小及数目)是衡量肿瘤细胞干性的金标准。成球能力是肿瘤干细胞体外鉴定的一个重要方法。其判断的是单个肿瘤细胞在合适的条件培养基中自我更新的能力,一般用细胞球形成效率(Sphere Formation Efficiency,SFE)表示,通过少量细胞能否持续形成3D肿瘤球来判断肿瘤细胞的增殖能力和细胞干性。传统的单层平面培养的肿瘤细胞则由于结构过于简单,缺乏合适的生理学载体和结构力学特性。与体内正常生长的细胞相距甚远。因此,在肿瘤的侵袭、转移的体外研究和药物的高通量筛选方面,肿瘤球已经逐步代替平面培养的肿瘤细胞成为肿瘤体外研究中常用的模型之一。
参考文献:
有限稀释法
有限稀释法是一种常用的克隆方法,是指将需要研究的组织、细胞群逐步制成悬液,稀释成一滴中最多含有一个细胞左右的浓度,再将其一滴加入培养基中进行培养的方法。将细胞株自培养孔内吸出并作细胞计数,用于单个细胞的分析实验。此外,现在一般多与平板培养法等其它方法混合使用,也可用于不适用噬菌斑形成法的病毒无性繁殖化及培养细胞的无性繁殖化的相关实验。
利用有限稀释分析可制作细胞成活曲线,即在接种相同数量细胞的培养瓶中,加入不同浓度的特定刺激物(例如抗原)或者外源细胞因子等,测定细胞对其刺激的反应程度与频率。用以评估细胞状态的最常用输出信号是细胞毒活性、细胞增殖或细胞因子产生的测量值。有限稀释分析的优点是可以监测包含多种类型应答细胞的复杂细胞混合物,其所分析的细胞群不需要进行分级分离,使得细胞和分子相互作用能够模拟体内情况。并且,该非侵入性的分析可重复多次进行,用健康个体的免疫细胞获得的结果在相对较长的时间内也是可重复的,实验操作更为简便。因此,有限稀释分析对于涉及定量免疫或造血细胞响应特定刺激等的临床实验也起到了重要作用。
本文中利用该方法实现用不同种类EVs来处理HCC细胞,更为直接详细地监测了HCC细胞的反应过程。并发现L–HCC–EVs处理的HCC细胞表现出其成瘤性显著增强,肿瘤发生率增加,肿瘤潜伏期缩短和肿瘤起始细胞预期频率增加等现象,从而证明了L–HCC–EVs促进肿瘤活性的显著效果。
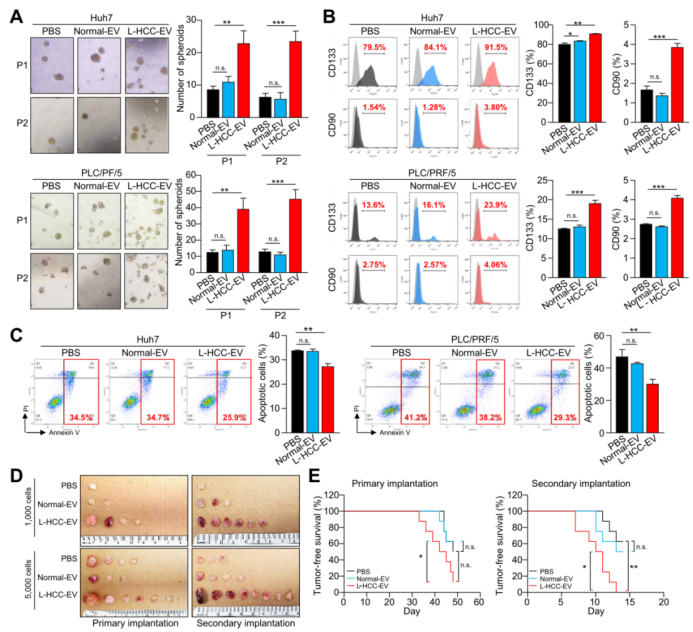
图2. 晚期HCC患者的循环EVs增强了HCC细胞的癌症干细胞特性

附图4. 晚期HCC患者的循环EVs增加了HCC细胞中的癌干细胞标记物
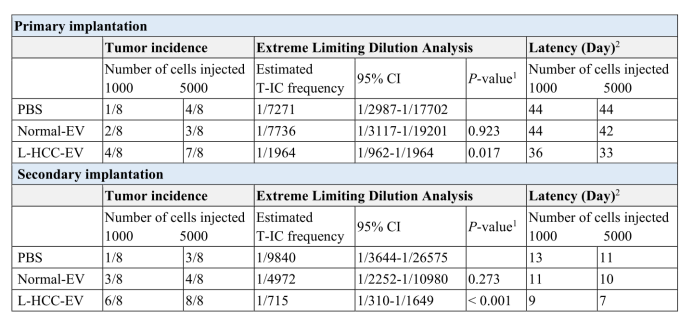
附表2. 正常和L-HCC-EV处理的PLC/PRF/5细胞的限制稀释和连续移植试验
3.肝癌患者循环EVs中pIgR上调
为了确定健康对照组和患者EVs之间生物活性的差异,作者对其进行蛋白质组学分析,并对EVs的蛋白质图谱进行了比较。与正常EVs相比,在L–HCC–EV中差异表达的基因(Fold change >2)中,作者选择了与HCC相关的pIgR进行了研究(图3A)。通过免疫印迹实验证实,E–HCC–EVs和L–HCC–EVs中pIgR显著上调(图3B)。同样的,作者在HCC患者队列的循环EVs中,也进一步证实pIgR水平显著增加(图3C)。同时,72%(18/25)的术后HCC患者,其EV-pIgR水平显著降低(图3D)。免疫金标记显示CD63+循环EVs表面存在pIgR(图3E);转移性HCC细胞的EVs中检测到的pIgR水平高于正常肝脏和非转移性细胞的EVs(图3F)。与此同时,在HCC细胞系中,pIgR在转录水平(图3G)和蛋白(图3H)水平上均显著增加。在植入具有转移性的MHCC97L肿瘤细胞的小鼠中,作者发现循环EV-pIgR水平在肿瘤发展过程中逐渐增加(图3I)。这些数据表明,肿瘤组织可能是EV-pIgR的主要来源,其水平可能是肿瘤发展的一个指标。与EV-pIgR类似,肿瘤组织中的总体pIgR mRNA表达相比非肿瘤组织显著上调(图3J)。相一致的是,56%(28/50)的HCC患者的肝脏肿瘤组织中pIgR 转录物上调(图3K)。在包含143对HCC组织样本的微阵列中,91.6%(131/143)的肿瘤组织中检测到强阳性(3级)和中等阳性(2级),而62.9%(90/143)的非肿瘤组织中检测到弱阳性(1级)或阴性染色(0级)(图3L-M)。此外,H评分(小编注:H-SCORE 即histochemistry score (组织化学评分)的缩写,是处理免疫组化结果的一种组织学评分方法,表示每张切片内阳性的细胞数量及其染色强度转化为相应的数值,达到对组织染色半定量的目的)显示肿瘤组织中pIgR的免疫反应性显著较高(图3M);在77.6%(11/143)的代表病例中也发现pIgR频繁地过度表达(图3N)。因此,L–HCC–EVs表面的pIgR可能介导了促进肿瘤细胞发生发展的关键作用。
拓展阅读
CSC(肿瘤干细胞)标志分子及主要通路
肿瘤是由形态和分子特性迥然不同的细胞构成的嵌合物,CSC是存在于肿瘤组织中的一小部分(约占1%~2%),同时具有干细胞和癌细胞的特征。除了自我更新和分化能力外,CSC 在移植到动物宿主中时还具有播种肿瘤的能力,它们在新宿主中增殖并形成新的病变。因此,CSC的“干性”并不在于它可以自我更新并分化成成熟的细胞类型(干细胞的经典标准),而在于它能够使致癌能力永久化。CSC被认为是肿瘤发育、形成转移瘤和复发的主要因素,CSC同时也具有化学耐药性和抗辐射性。CSC的这些特性与其特有的信号调控机制密切相关,寻找和鉴定特异性的CSC的表面标志物,从而识别肿瘤组织中的CSC,并进行相关信号调控机制的研究,将是肿瘤靶向治疗的关键。
CSC标志分子:CD133、CD44、CD90、ALDH1、ABCG2、核黄素等。涉及主要的信号通路:Wnt/β-catenin信号通路(在胚胎发育和胚胎干细胞增殖分化过程中起调节作用)、Notch信号通路(对调节细胞的增殖、分化、凋亡等有重要的作用,表达异常时会导致肿瘤的发生)、Hedgehog信号通路(高度保守,在调控胚胎干细胞和成体干细胞中有重要作用)。值得注意的是,CSC 表面标志物的表达是组织类型特异性的,甚至是肿瘤亚型特异性的。例如,CD44+CD24-/low Lineage 和 ALDH+ 被表征为乳腺 CSC;CD133+用于结肠、脑和肺;CD34+ CD8-用于白血病;CD44 +用于头部和颈部;CD90 +用于肝脏;CD44 +/CD24 + /ESA +用于胰腺 CSC。
本文中发现用L–HCC–EVs处理HCC细胞能够促进其CSC特性,促进肿瘤的恶性转化。
参考文献:
1.Doi:10.13865/icnki.cibmb.2015.10.02

图3. 在HCC患者中发现富含pIgR的循环EVs
4.pIgR促进了HCC患者来源EVs的促肿瘤作用
为了进一步的探究pIgR促进肿瘤发展的机制,作者针对于存在于EVs表面的pIgR(图3E),来探究pIgR的中和抗体是否能够阻断L–HCC–EVs的肿瘤促进作用。作者发现,与pIgR抗体联合治疗可阻断L–HCC–EVs对PLC/PRF/5细胞的克隆形成、迁移和侵袭的促进作用(图4A-B)。与此同时,与pIgR抗体共注射可显著阻碍由L–HCC–EVs诱导的p53-/-&Myc转导肝母细胞小鼠的肿瘤转移作用(图4C-F)。此外,pIgR抗体还消除了L–HCC–EVs促进体外自我更新、提高表达CD90、CD133的PLC /PRF /5细胞百分比(图4G-H)以及降低HCC细胞对索拉非尼的敏感性(图4I)的能力。在Huh7细胞中也观察到pIgR抗体抑制了L–HCC–EVs的增强活性(附图5)。这些结果表明,来自HCC患者的循环EVs是通过pIgR的功能来增强细胞的肿瘤干细胞特性的。
为了确定pIgR在EVs中的作用,作者通过CRISPR协同激活介质(SAM-pIgR)和EV靶向表达载体(XP-pIgR)在Huh7细胞中稳定表达pIgR(附图6A-B)(CRISPR SAM系统通过特异性激活pIgR基因在Huh7细胞内的转录,从而提高细胞内pIgR的表达量来提高EV里的装载量;而EV靶向表达系统是通过XPack克隆和慢病毒表达载体后将蛋白靶向介导至EV膜上或包装至EV/外泌体中,即特异性提高EV里的pIgR)。与从各自的对照组SAM-CTL和XP-CTL细胞收集的EVs相比,从SAM-pIgR和XP-pIgR细胞的条件培养基收集的EVs显示pIgR显著上调,同时也检测并保证了分离EVs的纯度和完整性(附图6A-D)。正如各种体外功能分析所揭示的那样,SAM-pIgR-EVs和XP-pIgR-EVs增强了PLC/PRF/5和Huh7细胞的癌症特性(图5A-C;附图7A-C)。通过添加pIgR抗体,SAM-pIgR- EVs和XP-pIgR-EVs促进Huh7细胞迁移和侵袭的增强效应被消除(附图7D-E)。XP-pIgR-EVs能够促进p53-/-&Myc转导的肝母细胞小鼠的肿瘤转移,添加pIgR抗体后这种促进作用也得到了消除(图5D-F)。此外,XP-pIgR-EVs还促进体外自我更新,增加表达CD90和CD133的PLC/PRF/5群体(图5G-H),并抑制HCC细胞对索拉非尼的敏感性(图5I)。一系列试验表明,与PBS或XP-CT-EVs处理的细胞相比,XP-pIgR- EVs处理的PLC/PRF/5细胞的致瘤性显著增强,伴随着肿瘤发生率增加,肿瘤潜伏期缩短和肿瘤起始细胞预期频率(即肿瘤启动细胞(tumor-initiating cell,TIC)的频率,大量肿瘤细胞群的TIC频率是用来区分遵循癌症干细胞模型的恶性肿瘤和不遵循的恶性肿瘤的标准之一)增加(附表3)。与初次异种移植相比,二次移植的XP-pIgR-EVs处理细胞的自我更新能力得到进一步增强(图5J)。XP-pIgR-EVs处理的细胞的无瘤生存率低于PBS或XP-CTL-EVs处理的细胞(图5K)。综上所述,这些发现表明EV-pIgR的功能与临床结果一致,显示了肝癌患者EV-pIgR上调。重要的是,这些数据证实了先前未发现的富含EV的pIgR在促进HCC侵袭性方面的作用。
拓展阅读
CRISPR SAM系统
CRISPR SAM(synergistic activation mediator)系统通过dCas9-VP64融合蛋白、改造过的sgRNA、RNA结合激活蛋白三个原件,实现了对多数细胞内源基因的特异性激活。该系统灵活方便,为研究基因功能提供了极为便利的工具。
CRISPR SAM可以通过导入几个简单的原件,即可实现对任何一个基因的特异性激活,即采用切割活性缺失的dCas9蛋白融合VP64转录激活蛋白,加上能与RNA结合蛋白MS2的sgRNA2.0,特异性识别并结合目标基因的启动子。MS2蛋白上连接p65和HSF1转录激活蛋白。通过多种转录激活蛋白的协同作用,能更好的模拟细胞内转录激活。
本文中还提到EV靶向表达载体(XP-pIgR),即应用了XPack技术。XPack多肽序列已经整合在了XPack克隆和慢病毒表达载体中,可将任一蛋白靶向介导至EV膜上或包装至EV/外泌体中,并高效地运输至靶细胞中发挥其生物学作用。(制作靶向外泌体,一般通过基因工程或表面化学方法来创建细胞特异性外泌体,在基因工程方法中,将靶向配体与外泌体膜蛋白遗传融合,然后在供体细胞中过表达。供体细胞因此产生展示靶向配体的基因工程外泌体。化学方法依赖于靶向配体与表面蛋白的生物缀合,但是在化学操作过程中可能发生表面蛋白失活或外泌体聚集。尽管存在局限性,但这两种方法均已成功实现。)
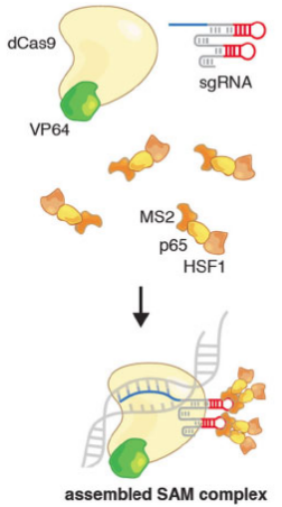
CRISPR SAM系统
参考文献:
1.Konermann,et al. Nature, 2015

图4. 抗pIgR抗体阻碍HCC患者来源的EVs增强HCC细胞癌症和肿瘤干细胞特性的能力
图5. 富含pIgR的EVs增强促进HCC癌症和癌症干细胞特性的作用

附图5. 抗pIgR抗体抑制肝癌患者EVs促进HCC细胞肿瘤和肿瘤干细胞特性的作用

附图6. 过表达pIgR的稳定克隆显示EVs中的pIgR表达增强
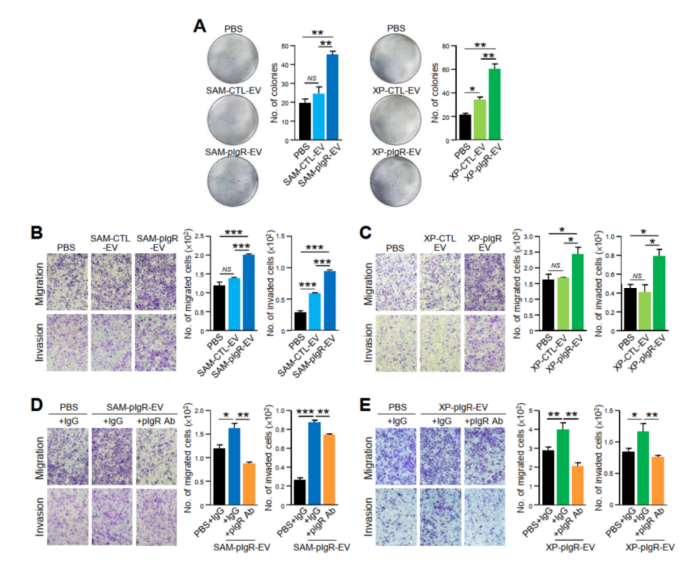
附图7. 提高pIgR表达的EVs增强促进HCC癌症和癌症干细胞特性的作用
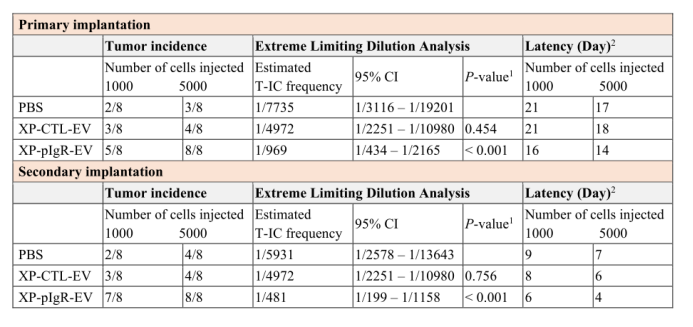
附表3. 对用XP-CTL-EVs和XP-pIgR-EVs处理的PLC/PRF/5细胞进行限制性稀释和连续移植试验
为了进一步地探索pIgR促进HCC侵袭性的潜在分子机制,作者在Normal-EVs和L–HCC–EVs处理的PLC/PRF/5和Huh7细胞中,分析了参与癌症干细胞和耐药性调节的基因表达(图6A)。结果显示,L–HCC–EVs显著增加了β-catenin表达,进一步说明L–HCC–EVs具有促进肿瘤恶性的潜力。TOP/FOP报告系统证明了L–HCC–EVs可以激活β-catenin(图6B)。接着,免疫荧光实验进一步证实了该结果,经pIgR高表达的EVs处理后,HCC细胞中β-catenin的核易位显著增加(图6C-D;附图8A-B)。值得注意的是,经过被内吞抑制剂(细胞松弛素D)处理后,L–HCC–EVs激活的β-连环蛋白核易位受到抑制,这表明EVs通过内吞被细胞摄取。
已有文献证明,β-catenin信号可调节肿瘤发生、癌症干细胞和化疗耐药性;PDK1的磷酸化可导致Akt的激活,Akt随后磷酸化GSK3β,能够促使β-catenin的核易位。作者发现,XP-pIgR-EVs可增加肿瘤组织PDK1、Akt和GSK3β的磷酸化(图6E,附图8C),这种激活又可被细胞松弛素D所阻断,这表明该激活过程需要细胞摄取的EVs来参与。同时,在PLC/PRF/5细胞中,作者使用Akt抑制剂IV和β-catenin抑制剂PRI-724处理细胞,降低了XP-pIgR-EVs诱导的Akt和GSK3β磷酸化作用(图7A),并消除了XP-pIgR-EVs对HCC细胞生长和运动的促进作用(图7B-D)。此外,与抑制剂共处理后,XP-pIgR-EVs增强PLC/PRF/5细胞体外自我更新能力、CD90+和CD133+细胞百分比(图7E-F)以及细胞对索拉非尼的敏感性(图7G)的作用显著减弱。这些结果表明,富含pIgR的EVs通过PDK1/Akt/GSK3β/β-catenin信号通路来促进癌症和癌症干细胞特性。
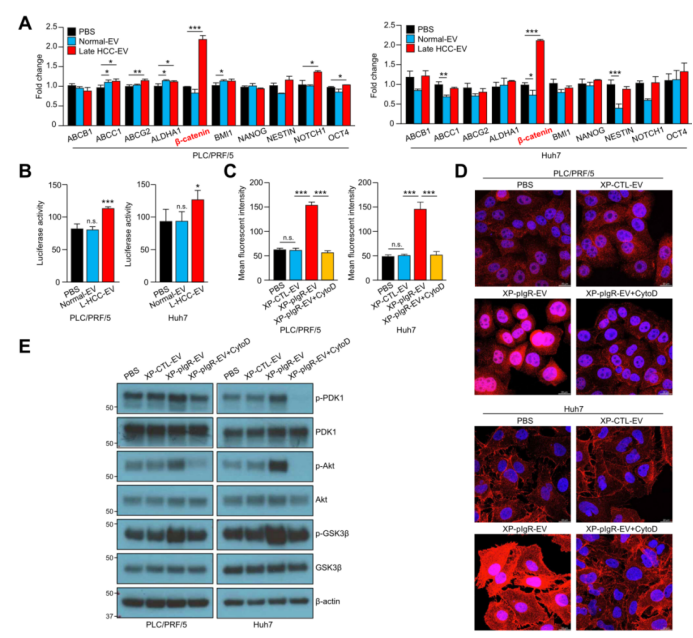
图6. 富含pIgR的EVs通过肝癌细胞PDK1/Akt/GSK3β信号通路激活β-连环蛋白信号
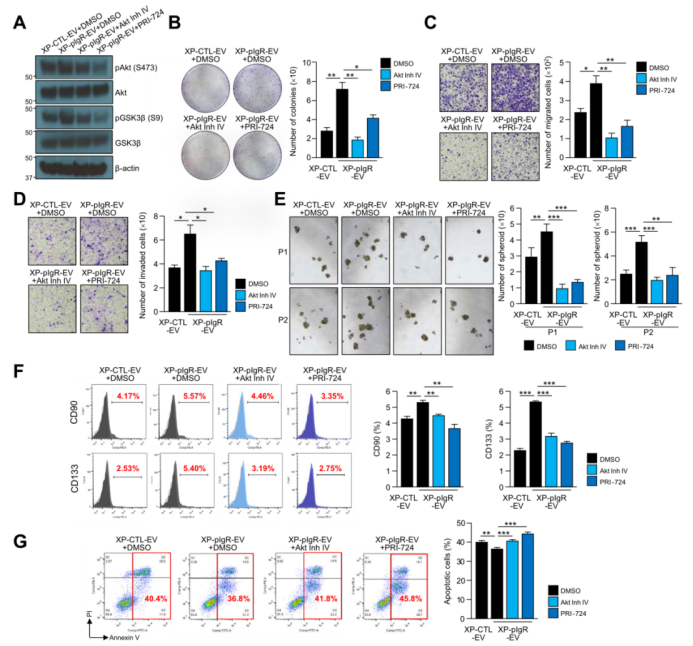
图7. Akt和β-连环蛋白抑制剂阻碍富含pIgR的EVs促进癌症和癌症干细胞特性

附图8. pIgR表达增强的EVs通过PDK1/Akt/GSK3β信号通路激活HCC细胞中的β-连环蛋白信号
6.pIgR中和抗体靶向EV-pIgR是肝癌潜在的治疗选择
在小鼠体内植入表达pIgR的PDTXs(病人来源的移植瘤),检测pIgR抗体和索拉非尼的治疗作用(图8A)。与载体治疗相比,pIgR抗体或索拉非尼的使用抑制了肿瘤生长(图8B)。值得注意的是,索拉非尼和pIgR抗体联合治疗对肿瘤形成的抑制作用最强(此过程中:作者没有观察到任何治疗组小鼠出现痛苦迹象或者体重显著变化)(图8C)。在接受索拉非尼和pIgR抗体联合治疗的小鼠中,解剖的肿瘤重量和尺寸显著减少(图8D)。同时,免疫组织化学分析显示,不同治疗组的肿瘤细胞本身的pIgR的表达没有变化,这表明pIgR抗体针对的不是内源性pIgR,而是通过靶向EV-pIgR来发挥作用。
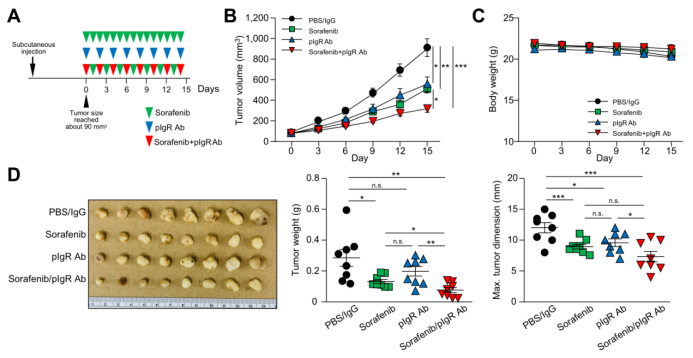
图8. 索拉非尼和pIgR中和抗体治疗可有效抑制患者来源的肿瘤异种移植的发展
总结
在本篇研究中,作者发现EV-pIgR能通过激活PDK1/Akt/GSK3β/β-catenin信号通路来促进肝癌细胞的侵袭性。首先,作者通过功能分析、实验性转移试验和肿瘤成球实验发现,HCC患者的循环EVs中pIgR水平升高并且促进了HCC细胞的侵袭性表型和癌症干细胞特性。为了阐明其中的分子机制,作者利用蛋白质组学图谱、免疫印迹和连续移植试验等方法证实,HCC患者EV-pIgR上调并促进HCC侵袭性。接着,作者进一步探索EV-pIgR是如何促进HCC细胞侵袭性,在免疫荧光染色和一系列信号抑制剂的处理后,发现富含pIgR的 EVs通过PDK1/Akt/GSK3β/β-catenin信号通路来促进癌症和癌症干细胞特性。最后,通过免疫组织化学分析,作者确认pIgR中和抗体能够靶向EV-pIgR来抑制肿瘤的形成。这也为癌症治疗提供了潜在的靶点和策略,使用中和抗体与索拉非尼或其他药物的联合治疗来阻断EV-pIgR可能是目前肝癌治疗的一个不错选择。
原文链接:https://doi.org/10.1016/j.jhep.2021.12.005
关注微信公众号代谢学人
了解更多代谢前沿资讯

https://m.sciencenet.cn/blog-3483272-1346880.html
上一篇:代谢学人--Cell Metabolism: 禁食让干细胞变身“睡美人”
下一篇:代谢学人--Nature Metabolism 6月刊代谢精选