ВЉЮФ
[зЊди]ЪВУДЪЧвѕЕРОњШКCSTЗжаЭЃЌВЛЭЌЕФЗжаЭДњБэФФаЉХЎадНЁПЕЮЪЬт
||
ШЫЬхФкЕФИїИіВПЮЛЃЌШчЦЄЗєЁЂПкЧЛЁЂГІЕРКЭвѕЕРЕШЃЌЖМЪЧЮЂЩњЮяЕФживЊЦмЯЂЕиЃЌетаЉЮЂЩњЮягыШЫЬхНЁПЕНєУмЯрЙиЃЌВЂФмЗДгГШЫЬхЕФМВВЁзДЬЌЁЃетаЉВПЮЛвђЪмЛљвђЁЂЛЗОГКЭЩњЛюЗНЪНЕШгАЯьЃЌОпгаЖРЬиЕФОњШКЬиеїЁЃ
ХЎадЩњжГЯЕЭГАќРЈТбГВЁЂЪфТбЙмЁЂзгЙЌКЭвѕЕРЕШжївЊЦїЙйЃЌвѕЕРЮЂЩњЬЌЖдХЎадЩњРэНЁПЕЁЂЩњжГНЁПЕКЭШбЩяЙ§ГЬжСЙиживЊЁЃЫцзХИпЭЈСПВтађММЪѕЕФНјВНЃЌвѕЕРЮЂЩњЮяМьВтвбБЛЙуЗКгІгУгкСйДВИОПЦИаШОЕФИЈжњеяЖЯКЭжЮСЦЃЌвдМАПЦбаЁЃ
вѕЕРЮЂЩњЮяШКЪЧЮЌЛЄвѕЕРНЁПЕЕФЙиМќЃЌНЁПЕЕФвѕЕРЩњЬЌжївЊгЩШщИЫОњзщГЩЃЌетаЉЯИОњЭЈЙ§ВњЩњШщЫсЁЂЙ§бѕЛЏЧтРДБЃЛЄвѕЕРЃЌВЂЪЭЗХЯИОњЫиЕШЛЏКЯЮявдЗРжЙгаКІЯИОњЖЈжВЁЃ
ШЛЖјЃЌвѕЕРЩњЬЌЯЕЭГЕФЪЇКтПЩФмЕМжТВЁдЬхЙ§ЖШЩњГЄЃЌв§ЗЂШчЯИОњадвѕЕРВЁ(BV)ЁЂадДЋВЅИаШО(STI)КЭЭтвѕвѕЕРФюжщОњВЁ(VVC)ЕШИДдгЕФвѕЕРИаШОЁЃ
вѕЕРЛЙПЩФмЪмЕНЖржжВЁдЬхШчШЫШщЭЗСіВЁЖО(HPV)КЭШЫРрУтвпШБЯнВЁЖО(HIV)ЕФИаШОЁЃСїааВЁбЇбаОПЯдЪОЃЌетаЉвђЫигыВЛСМНЁПЕНсЙћЕФЗчЯедіМггаЙиЁЃ
БОЮФжМдкЬНЬжвѕЕРОњШКЕФРраЭКЭвѕЕРЮЂЩњЬЌЕФживЊадЃЌВЂЬНЫїШчКЮЭЈЙ§ЮЂЩњЮяМьВтИЈжњИОПЦИаШОЮЪЬтЕФеяЖЯКЭжЮСЦЃЌДгЖјЮЊХЎадЩњжГЯЕЭГНЁПЕЬсЙЉИќЖрОЋзМЕФИіадЛЏЗНАИЁЃ
Part 01вѕЕРЮЂЩњЮяШКвѕЕРЮЂЩњЮяШКБЛЖЈвхЮЊдквѕЕРФкЖЈжГЕФЙВЩњКЭВЁдЮЂЩњЮяШКЃЌвѕЕРЮЂЩњЮяШКДгХЎадГіЩњЕФзюГѕМИИіаЁЪБПЊЪМОЭПЊЪМЖЈОгЃЌАщЫцХЎадвЛЩњЁЃ
ЫцзХВтађММЪѕЕФЦеМАЃЌНќФъРДЖдХЎадвѕЕРЮЂЩњЬЌНсЙЙгаСЫИќШЋУцЕФСЫНтВЂНјвЛВНзіЯИЗжЁЃ
✦ НЁПЕЕФвѕЕРОњШКвдШщИЫОњЮЊжїЕМ
зюжївЊЕФвѕЕРжжШКЪЧШщИЫОњЃЌдквѕЕРжавбМьВтГіГЌЙ§20жжШщЫсОњЃЌеМЯИОњШКТфЕФНќ70%ЁЃАќРЈЯТСаОњШКЕШЃК
-Lactobacillus crispatusЃЈОэЧњШщИЫОњЃЉ
-Lactobacillus gasseriЃЈИёЪЯШщИЫОњЃЉ
-Lactobacillus rhamnosusЃЈЪѓРюЬЧШщИЫОњЃЉ
-Lactobacillus inersЃЈЖшадШщИЫОњЃЉ
-Lactobacillus acidophilusЃЈЪШЫсШщИЫОњЃЉ
-Lactobacillus jenseniiЃЈеВЪЯШщИЫОњЃЉ
ДЫЭтЃЌЦфЫћЯИОњжжШКЕШвВДцдкгкНЁПЕИіЬхЕФвѕЕРжаЃЌР§ШчЯТСаМИжжЃК
-Prevotella biviaЃЈЦеРзЮжЪЯОњЃЉ
-Atopobium vaginaeЃЈвѕЕРАЂЭаВЈОњЃЉ
-Streptococcus aureusЃЈН№ЛЦЩЋСДЧђОњЃЉ
-BifidobacteriaceaeЃЈЫЋЦчИЫОњПЦЃЉ
-MobiluncusЃЈРяРЮЂЧђОњЃЉ
✦ вѕЕРОњШКБфЛЏЕФгАЯьвђЫи
ШЫРрвѕЕРЮЂЩњЮяШКзщЫцзХВЛЭЌЕФФъСфНзЖЮЗЂЩњБфЛЏЃЌАќРЈгЄЖљЁЂЧрДКЦкЁЂЛГдаКЭИќФъЦкЕШНзЖЮЁЃЖјЦфЫћЗНУцАќРЈМЄЫиЫЎЦНЁЂУтвпСІЁЂЯИОњИаШОЁЂПЙЩњЫижЮСЦЁЂдТОЁЂЩњЛюЗНЪНЕШЪЧгАЯьШЫРрвѕЕРЮЂЩњЮяШКЙЙГЩБфЛЏЕФГЃМћвђЫиЁЃ
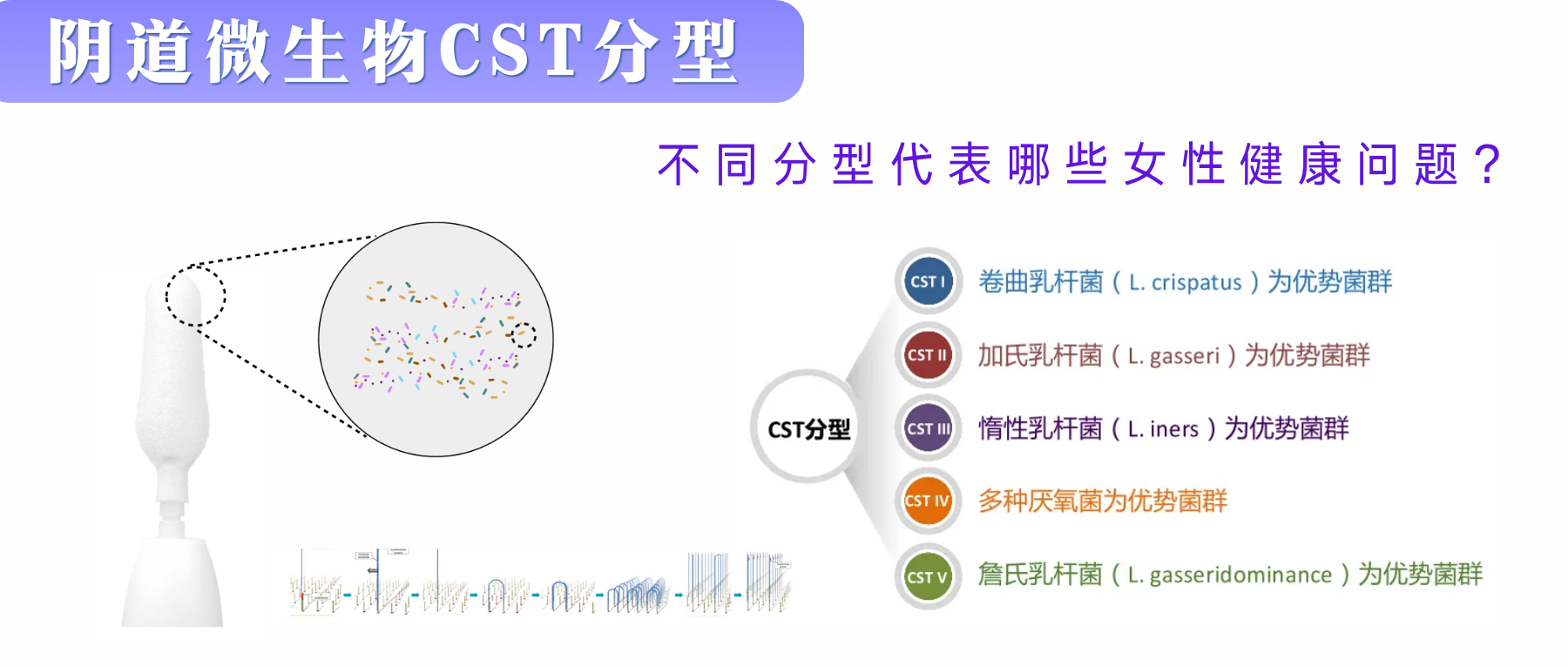
ЈЮхжжВЛЭЌРраЭвѕЕРОњШКЕФЬиеїдк2011ФъЃЌУРЙњRavelНЬЪкЪзДЮЭЈЙ§16S rRNAЛљвђЕФВтађММЪѕИљОнЮЂЩњЮязщГЩКЭЗсЖШЕФВЛЭЌЃЌНЋНЁПЕХЎадвѕЕРЮЂЩњЮяШКТфЖЈвхСЫ5жжВЛЭЌЕФШКТфзДЬЌРраЭЃЈcommunity-state types, CSTsЃЉЃЌВЂЗжБ№УќУћЮЊCST IЁЂIIЁЂIIIЁЂIVЁЂVЁЃЦфжагаЫФИівдШщИЫОњЮЊжїЁЃ

✦ CST-IЁЂCST-IIЁЂCST-VЁЊЁЊНЁПЕаЭ
НЁПЕвѕЕРжажївЊШщИЫОњЕФЯрЖдЗсЖШОіЖЈСЫЯИОњШКТфШКЕФРраЭЃЌОјДѓЖрЪ§НЁПЕг§СфХЎадЕФвѕЕРОњШКзщГЩжавдCST-I(ОэЧњШщЫсИЫОњ)ЁЂCST-II(МгЪЯШщЫсИЫОњ)ЁЂCST-V(еВЪЯШщЫсИЫОњ)етШ§жжРраЭНЯЮЊГЃМћЁЃ
CST-IаЭЃКдкЫљгаЕФвѕЕРОњаЭжаЃЌCST-IаЭБЛШЯЮЊЪЧзюНЁПЕЕФвЛжжРраЭЃЌЫќБэУївѕЕРДІгквЛИіЮШЖЈЕФзДЬЌЃЌЕжжЦВЁдОњФмСІНЯЧПЁЃ
CST-IаЭвдОэЧњШщИЫОњ(L. Crispatus)ЮЊжїЁЃОэЧњШщИЫОњФмВњЩњДѓСПЕФШщЫс(DаЭКЭLаЭЃЌЕЋбаОПБэУїD-ШщЫсЕФвжОњаЇЙћИќКУ)вдМАЙ§бѕЛЏЧтЃЌгаРћгквѕЕРЮЌГжШѕЫсадЕФЛЗОГЁЃОэЧњШщИЫОњЛЙПЩЗжУкПЙОњЛЏКЯЮяЃЌШчЯИОњЫиЁЂРрЯИОњЫиЕШЃЌДгЖјвжжЦВЁдОњЕФЩњГЄКЭЗБжГЁЃ
ДЫЭтЃЌОэЧњШщИЫОњЖдвѕЕРЩЯЦЄЯИАћЕФ№ЄИНзїгУзюЧПЃЌгыМгЪЯШщИЫОњЯрБШЃЌЫќИќФмОКељадвжжЦвѕЕРМгЕТФЩОњЕШгывѕЕРЩЯЦЄЯИАћЕФ№ЄИНЃЌзюжеЮЌГжвѕЕРЮЂЩњЬЌЕФЦНКтЁЃ
зЂЃКCST IаЭгжПЩЯИЗжЮЊСНИібЧаЭЃЌCST I-AаЭКЭCST I-BаЭЁЃСНепжЎМфЮЈвЛУїЯдЕФЧјБ№ЪЧI-AаЭжаОэЧњШщИЫОњЕФБШР§ИпгкCST I-BаЭЁЃ
ЫфШЛОэЧњШщИЫОњЗсЖШИќИпПЩФмИќгавцЃЌЕЋетСНжжбЧаЭЖМБэУївѕЕРДІгквЛИіБШНЯНЁПЕЕФзДЬЌЁЃашвЊзЂвтЕФЪЧИУжжРраЭдкдТОЦкЁЂдаЦкЁЂадЩњЛюЕШгАЯьЯТПЩФмЛсзЊБфЮЊCST IIIаЭЁЃ
CST-IIаЭЃКCST-IIаЭвВБЛШЯЮЊЪЧвЛжжНЁПЕЕФвѕЕРОњаЭЃЌИУжжРраЭЕФвѕЕРОњШКвдМгЪЯШщИЫОњ(Lactobacillus gasseri)ЮЊжїЁЃгыОэЧњШщИЫОњЯрЫЦЃЌМгЪЯШщИЫОњвВФмВњЩњD-ШщЫсЃЌЪЙвѕЕРЮЌГжШѕЫсадЕФЛЗОГЃЌВЂЩњГЩЙ§бѕЛЏЧтвжжЦдгОњЁЃ
ЫфШЛЫќУЧВњЩњЕФШщЫсКЌСПТдЕЭгкОэЧњШщИЫОњЃЌЕЋCSTIIаЭЖдВЁдЬхШдЯдЪОГіНЯЧПЕФЗРгљФмСІЁЃCST-IIаЭдкЮЇОјОЦкЕФХЎаджаНЯЮЊГЃМћЁЃЕБХЎадНјШыЮЇОјОЦкЃЌЬхФкДЦМЄЫиЫЎЦНж№НЅЯТНЕЃЌвѕЕРОњШКНсЙЙШнвзЗЂЩњБфЛЏЃЌДЫЪБЕФМгЪЯШщИЫОњдкЮЌГжвѕЕРЮЂЩњЬЌЦНКтжаПЩФмЗЂЛгживЊЕФзїгУЁЃ
зЂЃКCST-IIаЭдкФГаЉЧщПіЯТПЩзЊБфЮЊCST-IаЭ(ШчШбЩяЦк)ЁЃ
CST-VаЭЃКБЛШЯЮЊЪЧвЛжжНЁПЕЕФвѕЕРОњаЭЃЌвдеВЪНШщИЫОњ(Lactobacillus jensenii)ЮЊжїЁЃгыОэЧњШщИЫОњРрЫЦЃЌеВЪНШщИЫОњвВФмВњЩњD-ШщЫсЃЌНЕЕЭвѕЕРpHжЕЃЌЮЌГжШѕЫсадЛЗОГЃЌДЫЭтЛЙПЩЭЈЙ§№ЄИНгквѕЕРЩЯЦЄЯИАћКЭВњЩњЯИОњЫиРДЮЌГжвЛИівѕЕРЮЂЩњЬЌЕФЦНКтЁЃ
ЯрНЯЦфЫћCSTРраЭЃЌCST-VаЭНЯЮЊЩйМћЃЌбаОПБэУїИУжжРраЭНіеМВЛЕН10%ЁЃФПЧАЛЙЮДМћИУжжРраЭФмзЊБфГЩЦфЫћCSTаЭЕФБЈЕРЁЃ
✦CST-III аЭЁЊЁЊПЩФмдЄЪОвѕЕРУтвпСІЯТНЕ
CST-IIIаЭЃКвдЖшадШщИЫОњ(Lactobacillus iners)ЮЊжїЁЃЕБЖшадШщИЫОњгыЦфЫћШщИЫОњдквѕЕРФкЙВДцЪБЃЌЫќПЩФмВЮгыЮЌГжвѕЕРЮЂЩњЬЌЕФЦНКтЃЛЫќвВПЩФмдквѕЕРОњШКЪЇЕїКѓгыЖржжбсбѕОњЙВЭЌВЮгыЯИОњадвѕЕРВЁЕФЗЂеЙЙ§ГЬЁЃ
ЖшадШщИЫОњОпгаНЯШѕЕФЙ§бѕЛЏЧтВњЩњФмСІЃЌЗжУкЕФШщЫсжївЊЮЊLаЭЃЌвђДЫЖдвѕЕРЕФБЃЛЄзїгУВЛШчЦфЫћМИжжШщИЫОњ(ОэЧњЃЌМгЪЯКЭеВЪН)ЧПЁЃбаОПЗЂЯжЃЌгыЦфЫћжжРрЕФШщИЫОњЯрБШЃЌЖшадШщИЫОњЖдадДЋВЅИаШОКЭШбЩяВЂЗЂжЂЕФЗРЛЄФмСІНЯЕЭЁЃЫќгаИќИДдгЕФгЊбјашЧѓЃЌЪЧвѕЕРУтвпСІЯТНЕЕФБъжОЃЌПЩФмв§ЗЂвѕЕРИаШОЁЃ
зЂЃКCST IIIаЭгжПЩЯИЗжЮЊСНИібЧаЭЃЌCST III-AаЭКЭCST III-BаЭЁЃСНепжЎМфЕФЧјБ№ЪЧIII-AаЭЕФЖшадШщИЫОњЗсЖШБШIII-BаЭИќИпЁЃCST IIIаЭДњБэСЫвЛжжзЊБфЛђепВЛЮШЖЈзДЬЌЃЌШнвзЪеЕНЫожїздЩэЛђепЭтНчЛЗОГЬѕМўЯТЕФгАЯьДгЖјзЊБфГЩВЁРэзДЬЌЁЃ
✦CST-IVаЭЁЊЁЊвѕЕРЩњЬЌЪЇЕї
CST IVЕФЬиЕуЪЧШщИЫОњЕФЯрЖдЗсЖШЕЭЃЌЛьКЯЖржжМцадбсбѕОњЃЌбсбѕОњЕФЖрбљадКЭЗсИЛаддіМгЃЌАќРЈЦеРзЮжОњЪє(Prevotella)ЁЂМгЕТФЩОњЪє(Gardnerella)ЁЂОоаЭЧђОњЪє(Megasphaera)ЁЂЫЙФсЫЙОњЪєЃЈSneathiaЃЉЁЂЦјЧђОњЪє(Aerococcus)ЕШЁЃ
CST IVаЭЭЈГЃдкЯИОњадвѕЕРВЁЛМепжаНЯЮЊГЃМћЁЃИУжжРраЭгыадДЋВЅМВВЁЕФИаШОЗчЯедіМгЁЂШбЩяВЂЗЂжЂЁЂХшЧЛбзЁЂдчВњЁЂВЛдаВЛг§ЕШгаНЯЧПЕФЯрЙиадЁЃзЂЃКВЂВЛЪЧЫљгаЕФCST IVаЭвѕЕРОњШКЖМЪЧгЩЯрЭЌЕФЯИОњзщГЩЕФЁЃИљОнДцдкЯИОњБШР§ВЛЭЌЃЌCST IVаЭПЩБЛЗжЮЊAЁЂBЁЂCШ§ИібЧаЭЁЃIV-AаЭЕФЬиЕуЪЧвѕЕРМгЕТФЩОњКЭЯИОњадвѕЕРВЁЯрЙиЯИОњеМБШжаЕШЦЋИпЁЃIV-BаЭЕФЬиЕуЪЧвѕЕРФАЩњОњ(Atopobium vaginae)КЭвѕЕРМгЕТФЩОњ(Gardnerellavaginalis)еМгХЪЦЁЃA.vaginaeПЩгыG. vaginalisНсКЯПЩаЮГЩЩњЮяФЄЃЌетвВЪЧBVЗЂВЁМАИДЗЂЕФжївЊдвђЁЃ
IV-CгжПЩЯИЗжЮЊЮхИібЧаЭЃЈC0ЁЂC1ЁЂC2ЁЂC3ЁЂC4ЃЉЃЌIV-C0аЭОњШКЖрбљадзюИпЃЌЦфжаЦеРзЮжОњНЯЮЊГЃМћЁЃЦеРзЮжОњвВФмаЮГЩЩњЮяФЄЃЌЪЧСэвЛжжГЃгыЯИОњадвѕЕРВЁгаЙиЕФЮЂЩњЮяЁЃЂє-C1аЭвдСДЧђОњЮЊгХЪЦОњЃЌЂє-C2аЭвдГІЧђОњЮЊгХЪЦОњЃЌЂє-C3аЭвдЫЋЦчИЫОњЮЊгХЪЦОњЃЌЂє-C4аЭвдЦЯЬбЧђОњЮЊгХЪЦОњЁЃ
Part 02вѕЕРОњШКгыХЎадНЁПЕгыГІЕРЮЂЩњЮязщЯрБШЃЌвѕЕРЮЂЩњЮязщЕФЮяжжЖрбљадЯрЖдНЯЕЭЃЌвѕЕРЮЂЩњЮяШКЭЈГЃгЩМцадКЭзЈадбсбѕОњзщГЩЃЌвдШщИЫОњЮЊжїЕМЕФвѕЕРЮЂЩњЮяШКЪЧХЎадУкФђЩњжГЯЕЭГНЁПЕЕФжївЊОіЖЈвђЫиЁЃ
вдШщИЫОњЮЊжїЕМЕФНЁПЕШЫЬхвѕЕРжаЭЈГЃгавцЯИОњШКТфгыШЫРрЫожїжЎМфДцдкЙВДцЙиЯЕЃЌЭЈЙ§БЃЛЄЫожївѕЕРЛЗОГУтЪмВЁдЮЂЩњЮяЕФЖЈжВЃЌЭЌЪБЫожїЮЊЯИОњЩњГЄЬсЙЉгЊбјЁЃ
✦ вѕЕРЮЂЩњЮяЕФБЃЛЄзїгУ
вѕЕРЮЂЩњЮяШКдкБЃЛЄвѕЕРЩЯЦЄУтЪмВЁдЮЂЩњЮяЮлШОЗНУцЗЂЛгзХживЊзїгУЁЃетжжБЃЛЄЛњжЦЛљгкШ§жжЛњжЦЃК
1ЃЉЬьШЛЮЂЩњЮяШКгыВЁдЬхЕФОКељ
ШщИЫОњеГИНЕНвѕЕРЩЯЦЄЃЌЭЈЙ§ОКељадеМСьЙ§ГЬаЮГЩЕжПЙВЁдЮЂЩњЮяЕФБЃЛЄВуЁЃ
2ЃЉеыЖдетаЉВЛСМЮЂЩњЮяЕФПЙЮЂЩњЮяЮяжЪЕФЩњВњ
ЩњВњШ§жжВЛЭЌРраЭЕФЮяжЪЃКШщЫсЁЂЙ§бѕЛЏЧтКЭЯИОњЫиЁЃ
•ШщЫсЃКЮЌГжвѕЕРЕФpHжЕдкЫсадЃЌвжжЦВЁдЮЂЩњЮяЕФЩњГЄЁЃ
•Й§бѕЛЏЧтЃКгЩгкЦфбѕЛЏФмСІЖјОпгаПЙОњзїгУЁЃ
•ЯИОњЫиЃКЪЧЕААзжЪРДдДЕФЖОЫиЃЌОпгаПЙОњЙІФмЃЌЫќУЧЕФзїгУЪЧЭЈЙ§дкЯИОњЕФЯИАћжЪФЄжаВњЩњПзРДШмНтЛђЦЦЛЕЯИОњЕФЯИАћжЪФЄЁЃ
3ЃЉВЁдЮяжжЕФЙВОлМЏФмСІвдЬсИпПЙЮЂЩњЮяФмСІ
ВЁдЮЂЩњЮяБЛРДздЬьШЛвѕЕРЮЂЩњЮяШКЕФЯИОњАќЮЇЕФЛњжЦЁЃ
✦ вѕЕРОњШКЪЇКтгывЛаЉМВВЁЯрЙи
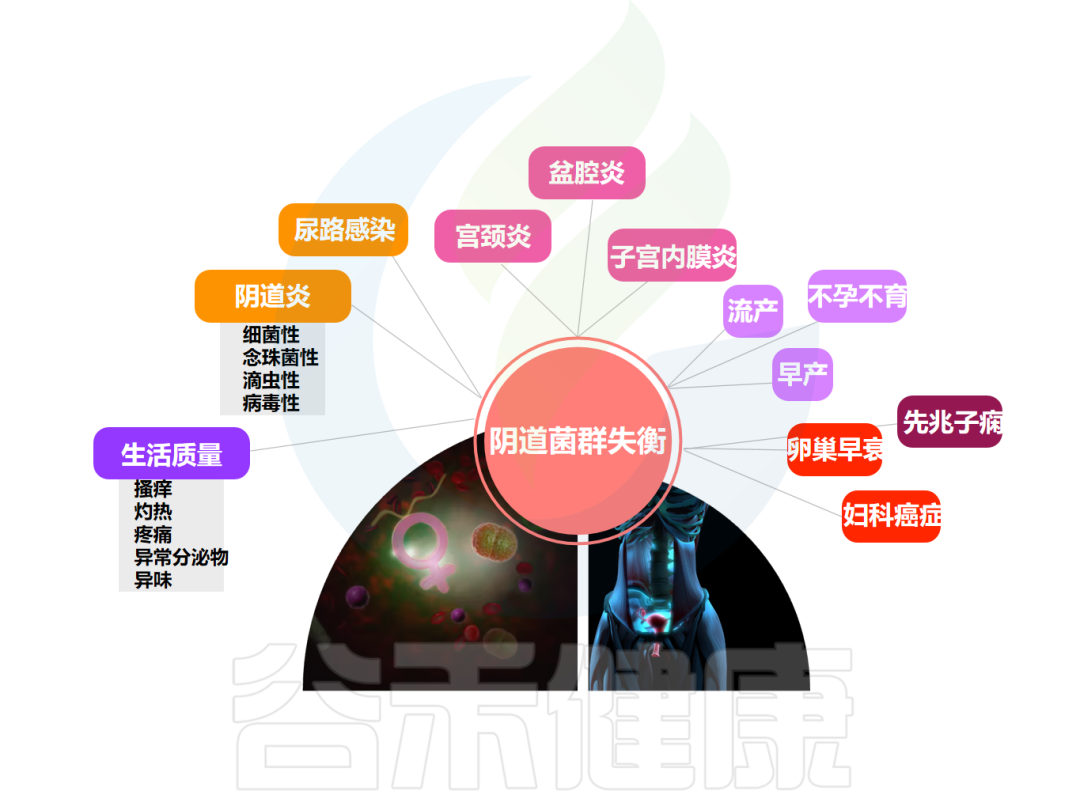
ШщИЫОњЕФЖЈжВКЭгХЪЦЪЧНЁПЕвѕЕРЮЂЩњЮяШКЕФЛљБОЬиеїЁЃе§ГЃЧщПіЯТЃЌЖўепДІгкЖЏЬЌЦНКтзДЬЌЁЃЕБвѕЕРЛЗОГЁЂЫожїЕШвђЫиЗЂЩњБфЛЏЕФЪБКђЃЌЩЯЪіЦНКтзДЬЌИФБфЃЌдђЮЊвѕЕРЮЂЩњЬЌЪЇЕїЁЃ
вѕЕРЯИОњБШР§ЪЇКтБЛШЯЮЊЛсЕМжТЩњжГЦїЙйШнвзЪмЕНИаШОЛђВЂЗЂжЂЁЃвѕЕРЮЂЩњЮяЕФзщГЩгыИаШОКЭДЋВЅШЫРрУтвпШБЯнВЁЖО(HIV)ЕФЗчЯедіМггаЙиЁЃВЂЧвИаШОЦфЫћадДЋВЅИаШОЕФЗчЯедіМгЃЌАќРЈСмВЁЁЂвТдЬхЁЂЕЮГцЁЂЕЅДП№хеюВЁЖО2(HSV-2)КЭУЗЖОЁЃЗЧзюМбЮЂЩњЮяШКЛЙгыШЫШщЭЗСіВЁЖО(HPV)ЕФЗЂВЁТЪКЭЛМВЁТЪвдМАЙЌОБЩЯЦЄФкСіБфЕФЯрЙиЗЂеЙКЭНјеЙвдМАЙЌОБАЉЗчЯедіМггаЙиЁЃ
вѕЕРЮЂЩњЮяШКЕФзщГЩЛЙгыФђТЗИаШОЁЂЭтвѕвѕЕРФюжщОњВЁКЭХшЧЛбзЕШМВВЁЯрЙиЁЃгажЄОнжЇГжвѕЕРЮЂЩњЮяШКЕФзщГЩгыЩњжГНЁПЕ(АќРЈдчВњЁЂздЗЂаддчВњКЭдчВњЬЅФЄдчЦЦ)жЎМфДцдкЙиСЊЁЃ
ЈЯИОњадвѕЕРбз
ЯИОњадвѕЕРбз(BV)ЪЧвЛжждкШЋЧђг§СфИОХЎжаЗЧГЃЦеБщЕФвѕЕРЮЂЩњЮяШКМВВЁЁЃШЋЪРНч23%ЈC29%ЕФХЎадЛМгаДЫВЁЁЃ
✦ ЯИОњадвѕЕРбзЕФЮЂЩњЮяЬиеї
ШщИЫОњзмЪ§ЕФМѕЩйЛђМБОчЯТНЕЃЌЭЌЪБМцадЛђзЈадбсбѕЮЂЩњЮяЕФХЈЖШдіМгЪ§БЖЃЌШчGardnerellaЁЂPrevotellaЁЂAtopobiumЁЂMobiluncusЁЂЫЋЦчИЫОњЁЂSneahiaЁЂLeptotrichiaЃЌвдМАЫѓзДбПАћИЫОњФПжаЕФвЛаЉаТЯИОњЃЌГЦЮЊBVЯрЙиЯИОњЁЃ
✦ ЯИОњадвѕЕРбзЕФЮЃКІ
ЯИОњадвѕЕРбз(BV)гыВЛСМЩњжГНЁПЕНсЙћЯрЙиЃЌР§ШчадДЋВЅИаШО(STI)КЭХшЧЛбз(PID)ЁЃДЫЭтЃЌдчВњ(PTB)ЁЂЕЭГіЩњЬхжиЁЂСїВњвдМАЦфЫћВЛСМВњПЦНсОжвВгыBVЯрЙиЁЃ
✦ ашбѕадвѕЕРбзвВДцдкЩњЬЌЪЇЕї
ДЫЭтЃЌСэвЛжжГЦЮЊашбѕадвѕЕРбз(AV)ЕФЩњЬЌЪЇЕїМВВЁОГЃгыBVЯрЛьЯ§ЁЃетЪЧвђЮЊЃЌСНепЖМгывѕЕРЮЂЩњЮяЕФCST-IVЯрЫЦЃЌМДШБЗІДѓСПЕФШщИЫОњЃЌpH>4.5ЁЃ
ШЛЖјЃЌИљОнЮЂЩњЮяЖрбљадЖдетСНжжЧщПіНјааСЫЧјЗжЁЃ BVЪЧжИДцдкбЯИёбсбѕОњЃЛЖјAVЪЧжИДцдкашбѕГІЕРЯИОњЃЌАќРЈДѓГІИЫОњЁЂН№ЛЦЩЋЦЯЬбЧђОњЁЂBзхСДЧђОњ(ЮоШщСДЧђОњ)ЛђГІЧђОњЁЃ
ашбѕадвѕЕРбзГ§СЫОпгаВЁдЬхИДдгЕФЬиЕуЭтЃЌЛЙвзКЯВЂЦфЫћвѕЕРИаШОЁЃAVВЛНіПЩЕМжТЛМепЭтвѕвѕЕРВЛЪЪЃЌЛЙгыХшЧЛбзжЂадМВВЁЁЂВЛдажЂвдМАСїВњЁЂдчВњЁЂЬЅФЄдчЦЦЁЂШоУЋФЄбђФЄбзЁЂаТЩњЖљИаШОЁЂВњШьИаШОЕШВЛСМШбЩяНсОжгаЙиЁЃ
ЈвѕЕРЮЂЩњЮягыдчВњ
дНРДдНЖрЕФжЄОнБэУївѕЕРЮЂЩњЮязщгыздЗЂаддчВњЗчЯегаЙиЁЃ
вѕЕРЮЂЩњЮяШКдкШбЩяНЁПЕКЭНсОжжаЦ№зХживЊзїгУЃЌвѕЕРОњШКЪЇЕїЕФдіМг(ЭЈГЃвдCST IVОњШКЕФЗсЖШНЯИпКЭШщЫсИЫОњЕФЗсЖШНЯЕЭЮЊЬиеї)ЕМжТШбЩяВЂЗЂжЂКЭдчВњЗчЯедіМгЁЃ
✦ зудТЗжУфЕФИОХЎвѕЕРЮЂЩњЮяШКЮШЖЈ
зудТЗжУфИОХЎЕФвѕЕРЮЂЩњЮяШКТфЭЈГЃЪЧЮШЖЈЕФЃЌдкЛГдадчЦквдШщИЫОњЮЊжїЃЛЖјОРњдчВњЕФХЎадЭЈГЃвѕЕРОњШКвдбсбѕОњЮЊжїЁЃ
дкДѓЖрЪ§зудТЗжУфжаЃЌвѕЕРЮЂЩњЮяШКЕФЬиЕуЪЧКёБкОњУХГЩдБеМгХЪЦЃЌЗХЯпОњУХЁЂБфаЮОњУХЁЂФтИЫОњУХКЭЫѓИЫОњУХГЩдБЕФЗсЖШНЯЕЭЃЌЖјдкдчВњЕФЧщПіЯТЃЌКёБкОњЕФЪ§СПМѕЩйЁЃ
✦ ЕЭЗсЖШЕФШщИЫОњгыдчВњЗчЯедіМгЯрЙи
ЖджСЩйШ§жжВЛЭЌCSTжаЕФвѕЕРЮЂЩњЮязщНјааЗжРрвдЦРЙРдчВњЗчЯеЕФзнЯђбаОПЁЃЫљга17ЯюбаОПОљдк2014ФъжС2021ЦкМфЗЂБэЃЌАќРЈ38-539Р§ШбЩяКЭ8-107Р§дчВњЁЃгыДрШщИЫОњеМгХЪЦЕФХЎадЯрБШЃЌОпгаЁАЕЭШщИЫОњЁБвѕЕРЮЂЩњЮязщЕФХЎаддчВњЗчЯедіМгЃЈOR 1.69ЃЌ95%CI 1.15ЈC2.49ЃЉЁЃ
ЭјТчмінЭЗжЮіжЇГжЮЂЩњЮязщПЩвддЄВтдчВњЃЌЦфжаЕЭЗсЖШЕФШщЫсОњгызюИпЕФЗчЯеЯрЙиЃЌЖјL. crispatusгХЪЦОњШКЕФдчВњЗчЯезюЕЭЁЃ
ЈвѕЕРЮЂЩњЮягыВЛдадНРДдНЖрЕФжЄОнБэУїЃЌУПИіХЎадЖРгаЕФвѕЕРЮЂЩњЮяШКдкОіЖЈЩњжГНЁПЕаэЖрЗНУцЦ№зХживЊзїгУЁЃ
✦ гыВЛдаЯрЙиЕФвѕЕРОњШКЪЇЕї
баОПБэУїЃЌL. iners ЁЂL . crispatusЁЂL. gasseriПЩвдЧјЗжЬиЗЂадВЛдаХЎадгыНЁПЕХЎадЛђвѕЕРВЁЛМепЁЃ
ШщИЫОњжїЕМЕФвѕЕРОњШКЭЈГЃБЛЪгЮЊе§ГЃЕФБъжОЁЃШЛЖјЃЌаэЖрбаОПБэУїЃЌВЂЗЧЫљгаРраЭЕФШщИЫОњЖМЪЧгавцОњЃЌР§ШчЃЌL.crispatus ЫЦКѕОпгагавцЬиадЃЌЖјL.iners дђУЛгаЁЃ
ЛМгаЬиЗЂадВЛдаЕФХЎадЫЦКѕИќШнвзГіЯжвѕЕРОњШКЪЇЕїЁЃбаОПШЫдБНЋвѕЕРЮЂЩњЮяШКЗжЮЊСНРрЃКЕЭШщЫсИЫОњвѕЕРЮЂЩњЮяШК(LL-VMB)КЭИпШщЫсИЫОњвѕЕРЮЂЩњЮяШК(HL-VMB)ЁЃбаОПШЫдБПЊЪМЦРЙРХЎадВЛг§гывѕЕРЮЂЩњЮяШКжЎМфЕФЭГМЦЙиСЊЃЌНсЙћШчЯТЃК
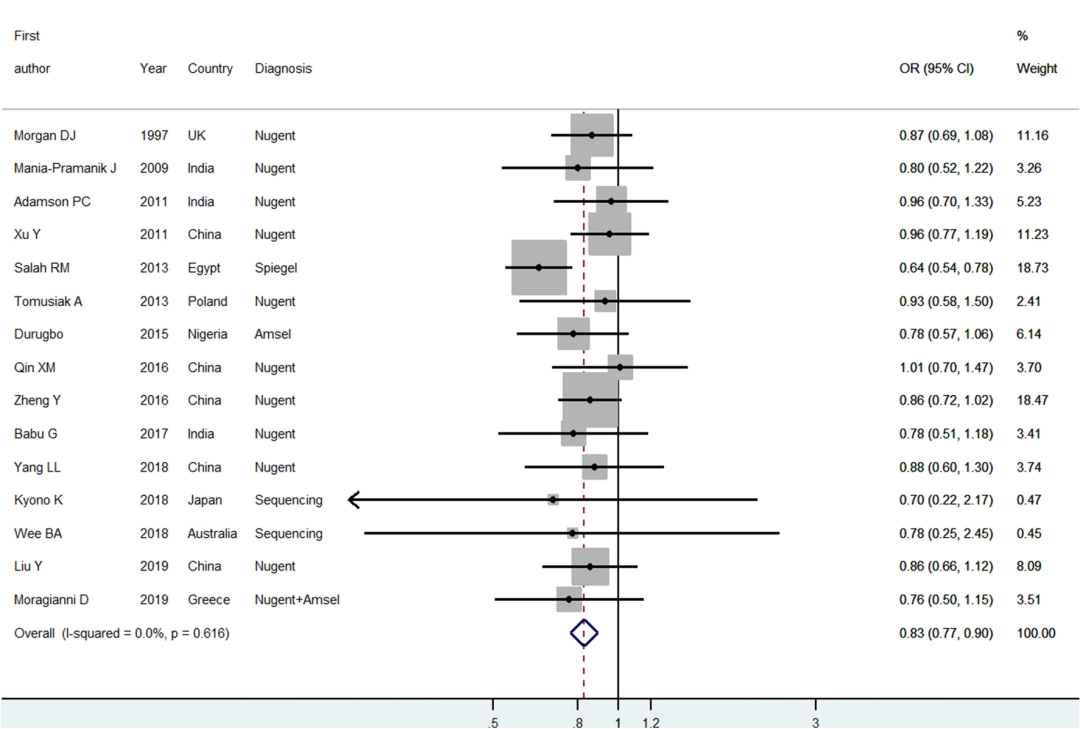
DOI: 10.1007/s00404-020-05675-3
Ъ§ОнЯдЪОЃЌЯИОњадвѕЕРбзгыХЎадВЛдажЂГЪе§ЯрЙиЃЌВЂЧвЯИОњадвѕЕРбзбєадепЕФгАЯьДѓгкЯИОњадвѕЕРбзжаМфжЕепЁЃ
✦ ЕЭШщЫсИЫОњвѕЕРЮЂЩњЮяШКЛђЯИОњадвѕЕРВЁ ПЩФмЖдЪмОЋЙ§ГЬВњЩњгАЯь
ХЎадВЛдажЂПЩИљОнВЛЭЌЕФБъзМЗжЮЊВЛЭЌЕФРраЭЃЌЦфжагывѕЕРЮЂЩњЮяШКЕФЙиСЊПЩФмгаЫљВЛЭЌЁЃДгВЁвђбЇЕФНЧЖШРДПДЃЌЪфТбЙмадВЛдажЂЪЧгывѕЕРЮЂЩњЮяШКЯрЙиЕФзюГЃМћМВВЁЁЃ
гЩЯИОњадвѕЕРбзв§Ц№ЕФТ§адбзжЂЗДгІвВПЩФмЪЧЪфТбЙмеГСЌЕФдвђЃЌжСЩйЪЧВПЗждвђЁЃ
✦ вѕЕРЮЂЩњЮяШКЖдЛГдагАЯьЕФЦфЫћбаОП

ЈвѕЕРЮЂЩњЮягыЖрФвТбГВзлКЯжЂЖрФвТбГВзлКЯеї(PCOS)БЛЙуЗКЖЈвхЮЊвЛжжФкЗжУкКЭДњаЛЮЩТвЃЌАщгаалМЄЫиЙ§Жр(ЖрУЋжЂЛђИпалМЄЫибЊжЂ)КЭТбГВЙІФмеЯА(ЩйХХТбЛђЖрФв)ЕФЬхеїКЭжЂзДЃЌШчНёБфЕУдНРДдНГЃМћЁЃ
гЩгкНЁПЕХЎадЕФЮЂЩњЮяШКТфДІгкЖЏЬЌЦНКтзДЬЌЃЌвђДЫВЛЦНКтЕФЮЂЩњЮяШКзщГЩБЛШЯЮЊгыЖрФвТбГВзлКЯжЂХЎадгаЙиЁЃаэЖрбаОПШЫдБвбЙуЗКжЄУїЃЌPCOSЖЏЮяФЃаЭКЭЛМгаPCOSЕФХЎаджаЛсЗЂЩњЮЂЩњЮяШКзщГЩЕФБфЛЏКЭОњШКЪЇЕїЁЃ
✦ ЖрФвТбГВзлКЯеїЛМепЕФШщИЫОњЯджјМѕЩй
ОнБЈЕРЃЌЧрДКЦкЧАХЎадКЭОјОКѓХЎадЕФвѕЕРЮЂЩњЮязщДцдкКмДѓВювьЁЃетжївЊЪЧгЩгкЯТЩњжГЕРЮЂЩњЮязщЛсЪмЕНФъСфЁЂадМЄЫиЫЎЦНЁЂЩњЛюЯАЙпЕШЕФгАЯьЁЃ
ЦфжаЃЌдТОВЛЙцТЩКЭМЄЫиЫЎЦНвьГЃБЛШЯЮЊЪЧЕМжТPCOSХЎадвѕЕРЮЂЩњЮязщИФБфЕФСНИіжївЊдвђЁЃе§ГЃЕФдТОАщЫцзХДЦМЄЫиКЭдаМЄЫиЕФЙцТЩБфЛЏЃЌЛсДјЖЏЩњжГЕРБэЦЄЯИАћЕФЩњРэБфЛЏЃЌЮЌГжЮЂЛЗОГЃЈАќРЈЦНКтЕФЮЂЩњЮяШКТфЃЉЕФЦНКтЁЃЯрЗДЃЌPCOSХЎадЕФдТОВЛЕїЛсЕМжТЯТЩњжГЕРЮЂЩњЮязщЕФзщГЩЗЂЩњБфЛЏЁЃ
ЭЈЙ§ 16S rRNA ЛљвђВтађЗжЮіЕФ 194 ИіЮЂЩњЮябљБОЕФНсЙћ БэУїЃЌPCOS КЭНЁПЕХЎаддквѕЕРЮЂЩњЮязщКЭЙЌОБЙмЮЂЩњЮязщжаЕФРрШКЗсЖШДцдкЯджјВювьЁЃдкЖрФвТбГВзлКЯжЂХЎаджаЃЌНсЙћЗЂЯжШщИЫОњЕФГЩЗжЯджјМѕЩйЁЃ
СэвЛЗНУцЃЌЦфЫћвЛаЉЮЂЩњЮяШКЃЌШчвѕЕРМгЕТФЩОњ (Gardnerella vaginalis)ЁЂЩГблвТдЬх (Chlamydia trachomatis) КЭЦеРзЮжЪЯОњ (Prevotella) ЭЌЪБдіМгЁЃДЫЭтЃЌетаЉдіМгЕФЮЂЩњЮяШКБЛШЯЮЊЪЧвѕЕРКЭЙЌОБЙмжаЧБдкЕФжТВЁРрШКЁЃ
✦ PCOSжаЕФЮЂЩњЮязщКЭадМЄЫи
баОПБэУїЃЌадМЄЫигАЯьЮЂЩњЮязщЕФзщГЩЃЌАќРЈГІЕРЮЂЩњЮязщКЭвѕЕРЮЂЩњЮязщЁЃМЄЫиЫЎЦНВЛЦНКтПЩФмгыЖрФвТбГВзлКЯжЂЕФЮЂЩњЮязщЁАЪЇКтЁБгаЙиЁЃ
дНРДдНЖрЕФбаОПБэУїЃЌДЦМЄЫиЖдгкНЈСЂХЎадЦНКтЕФЮЂЩњЮяШКТфНсЙЙжСЙиживЊЁЃжкЫљжмжЊЃЌДЦМЄЫидкдіМгвѕЕРЩЯЦЄЯИАћЬЧдЕФВњЩњВЂЫцКѓДйНјШщИЫОњЕФЩњГЄЗНУцЗЂЛгзХЙиМќзїгУЁЃОЁЙмгабаОПБэУїИпЕэЗлвћЪГЪЧШщЫсОњеМжїЕМЕиЮЛЕФдвђЃЌЕЋДЦМЄЫиШдШЛБЛШЯЮЊЪЧетвЛЙ§ГЬЕФКЫаФвђЫиЁЃ
ИќживЊЕФЪЧЃЌЮЂЩњЮязщЛЙЕїНкЖрФвТбГВзлКЯжЂЕФадМЄЫиЁЃОнБЈЕРЃЌЛМгаPCOSЕФХЎадЬхФкалМЄЫиЫЎЦННЯИпгыДњаЛЪЇЕїгаЙиЁЃгЩгкадМЄЫиЪмЕНЮЂЩњЮязщЕФгАЯьЃЌвђДЫПЩвдКЯРэЕиЭЦВтЮЂЩњЮяЪЇКтЪЧЕМжТЖрФвТбГВзлКЯжЂЕФдвђЁЃЖрЯюбаОПБЈИцГЦЃЌЖрФвТбГВзлКЯжЂгыГІЕРЮЂЩњЮяШКзщГЩЕФвьГЃВЈЖЏгаЙиЁЃетаЉВЈЖЏПЩвдИХРЈЮЊІТЖрбљадЕФвьГЃБфЛЏКЭІСЖрбљадЕФЯТНЕЃЌВЛНіАќРЈЮяжжЗсИЛЖШЃЌЛЙАќРЈЯЕЭГЗЂг§ЖрбљадЁЃ
ИќживЊЕФЪЧЃЌадМЄЫиЁЂвѕЕРвдМАГІЕРЮЂЩњЮяШКжЎМфЕФЯрЛЅзїгУЪЧвЛИіЖрВНжшЕФЙ§ГЬЁЃГІЕРЮЂЩњЮяШКЕїНкДЦМЄЫиЫЎЦНЃЌДЦМЄЫиЕїНквѕЕРЮЂЩњЮяШКЁЃвђДЫЃЌвьГЃЕФГІЕРЮЂЩњЮязщЛђвѕЕРЮЂЩњЮязщПЩФмдк PCOS жаЯрЛЅгАЯьЃЌАќРЈЕїНкЮЂЩњЮязщЕФзщГЩКЭЕїНкМЄЫиЕФБфЛЏЁЃУтвпЮШЬЌгаРћгкХЎадНЈСЂНЁПЕЕФЮЂЛЗОГЁЃ
▸ ЮЊЪВУДвЊНјаавѕЕРОњШКМьВтЃП
1. ШЋУцСЫНтОњШКНсЙЙЃКИпЭЈСПЖўДњВтађКЭ 16S ВтађФмЙЛИќШЋУцЁЂОЋШЗЕиЗжЮівѕЕРОњШКЃЌЬсЙЉИќЗсИЛЕФаХЯЂЃЌгажњгкЩюШыСЫНтвѕЕРЮЂЩњЬЌЛЗОГЁЃ
2. дчЦкЗЂЯжвьГЃЃКгажњгкдчЦкЗЂЯжЧБдкЕФОњШКЪЇКтЃЌЮЊЯИОњадвѕЕРбзМАВЛСМШбЩяНсЙћЕФеяЖЯКЭИЩдЄЬсЙЉвРОнЁЃ
3. ИіадЛЏжЮСЦЃКИљОнМьВтНсЙћПЩвджЦЖЈИќгаеыЖдадЕФжЮСЦЗНАИЃЌЬсИпжЮСЦаЇЙћЁЃ
Part 03ЙШКЬвѕЕРОњШКМьВтММЪѕвдЗжзгЩњЮябЇКЭDNAВтађММЪѕЕФЗЂеЙЮЊЩњжГЕРЮЂЩњЬЌбаОПЬсЙЉСЫПЩППЕФММЪѕжЇГжЃЌЭЈГЃВЩгУ16S rRNAЛљвђРЉдізгНјааВтађЁЃ
▸ ЙШКЬвѕЕРОњШКМьВт
ЙШКЬНЁПЕдЫгУИпЭЈСПВтађММЪѕЃЌЕУЕНвѕЕРжаДѓЖрЪ§ЮЂЩњЮяЕФаХЯЂЃЌВЂЭЈЙ§ЩњаХЭГМЦбЇЖдЮЂЩњЮяОњШКЪ§ОнНјааДІРэЃЌЭЈЙ§ЗжЮівѕЕРЮЂЩњЮяЕФзщГЩМАЯрЖдЗсЖШЃЌЖдвѕЕРЮЂЩњЮяШКТфзДЬЌРраЭ(CST)НјааЗжаЭЃЌПЩАяжњМрВтКЭЗжЮіХЎадвѕЕРЕФНЁПЕзДПіЃЌВЂЖдВЛЭЌМВВЁМАЬѕМўЕФЗжзщНјааCSTОлРрЃЌЗжЮіВЛЭЌЗжзщЬѕМўЯТЕФвѕЕРОњШКЕФЬиеїВювьЃЌЮЊСйДВПЦбаЗжЮізіжИЕМЁЃ
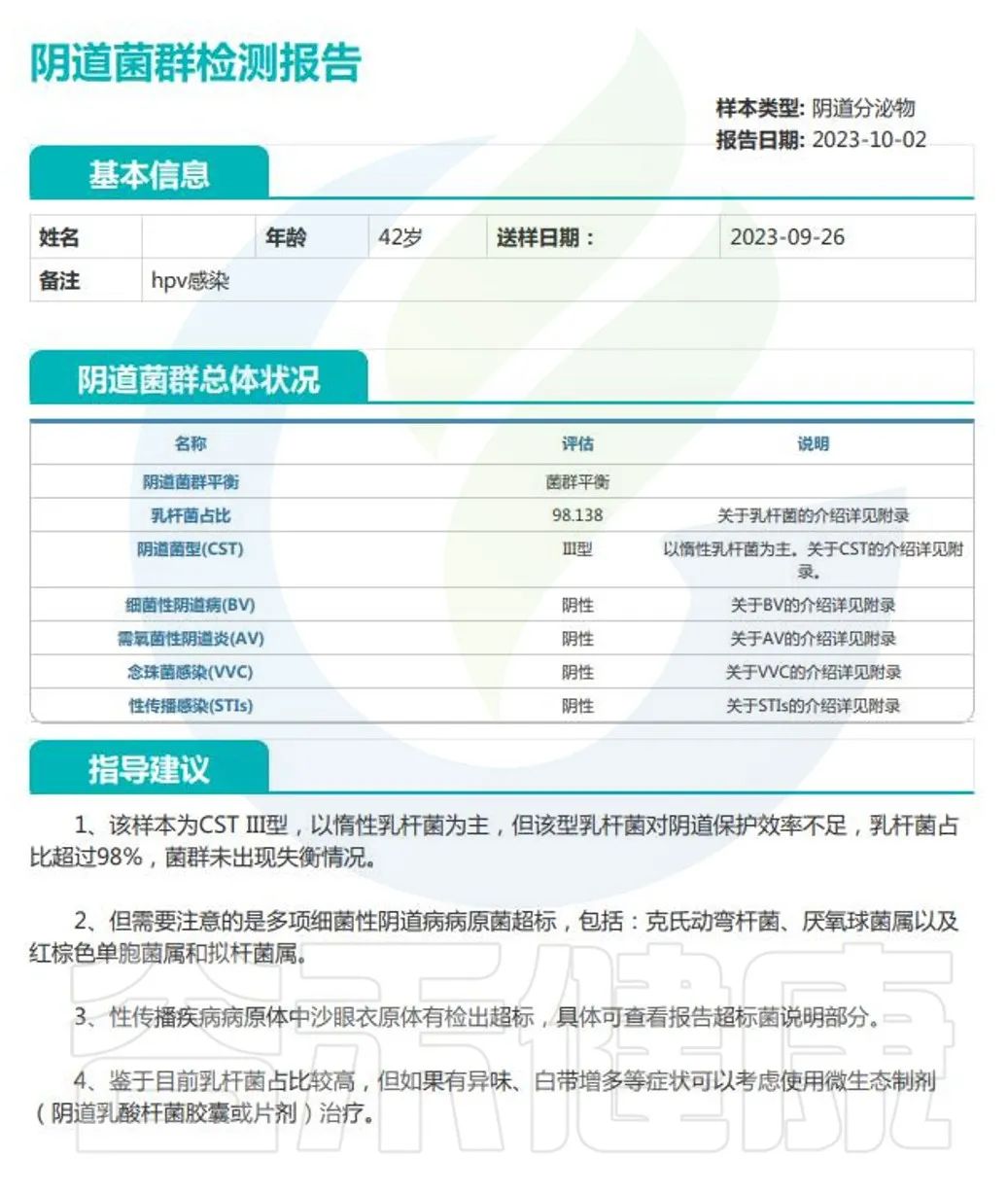
▸ УцЯђШЫШКЬиЕуМАНтОіЮЪЬт
1. УцЯђгаВЛСМШбЩяЪЗЛђвЩЫЦЯИОњадвѕЕРбзЕФШЫШКЃКАяжњетаЉШЫШКИќзМШЗЕиЦРЙРвѕЕРЮЂЩњЬЌзДПіЃЌевГіПЩФмЕМжТВЛСМШбЩяНсЙћЕФдвђЁЃ
2. НтОіЮЪЬтЃКУїШЗОњШКЪЇКтЧщПіЃЌЮЊжЮСЦЬсЙЉПЦбЇвРОнЃЌЬсИпШбЩяГЩЙІТЪЃЌИФЩЦХЎадЩњжГНЁПЕЁЃ
ашвЊзЂвтЕФЪЧЃЌдкЪЕМЪгІгУжаЃЌгІНсКЯСйДВжЂзДЁЂЦфЫћМьВщНсЙћЕШНјаазлКЯЗжЮіКЭХаЖЯЁЃ
Part 04ЙигкЯИОњадвѕЕРбзЕФжЮСЦ▸ ЯИОњадвѕЕРбзМЋвзИДЗЂ
ЯИОњадвѕЕРбзЪЧвЛжжГЃМћЕФИОПЦМВВЁЃЌвдвѕЕРФкЯИОњЪЇКтЮЊжївЊЬиеїЁЃОЁЙмЕБЧАЕФжЮСЦЗНЗЈПЩвдгааЇЛКНтжЂзДЃЌЕЋИУВЁжЂЕФИДЗЂТЪвРШЛНЯИпЁЃИДЗЂЕФдвђЖржжЖрбљЃЌАќРЈЕЋВЛЯогкПЙЩњЫижЮСЦКѓЕФОњШКЪЇКтЁЂИіШЫЮРЩњЯАЙпЁЂМЄЫиЫЎЦНБфЛЏвдМАадааЮЊЕШвђЫиЁЃ
вђДЫЃЌЖдгкЯИОњадвѕЕРбзЕФЙмРэЃЌГ§СЫжЮСЦГѕЗЂИаШОЭтЃЌИќашжиЪгМВВЁЕФГЄЦкдЄЗРКЭПижЦВпТдЁЃвѕЕРЮЂЩњЮяЕФЩњЬЌЦНКтЖдгкжЮСЦМЋЮЊживЊЁЃ
▸ ЙизЂвѕЕРЮЂЩњЮягажњгкЬсИпжЮгњТЪ

вЛЯюбаОПФЩШыСЫ46УћНгЪмМзЯѕпђжЮСЦЕФЯИОњадвѕЕРбзЛМепЃЌЦфжаНі20УћЛМепБЛжЮгњЃЌдкжЮСЦЧАКѓМьВтвѕЕРОњШККѓЗЂЯжЃКдкжЮгњЕФЛМепжаЃЌЦфдкМзЯѕпђжЮСЦЧАЖшадШщИЫОњИЛМЏЃЌВЂЧвдкжЮСЦКѓБЃГжНЯИпЕФЗсЖШЁЃ
ЖшадШщИЫОњ(L.iners)жїЕМЕФвѕЕРОњаЭгыНЯВюЕФПЙЯИОњадвѕЕРбз(BV)ФмСІгаЙиЃЌЧвГЃЙцМзЯѕпђжЮСЦВЂВЛЛсМѕЩйL.inersЕФЗсЖШЁЃЖјОэЧњШщИЫОњ(L.crispatus)гаНЯИпПЙBVЕФЧБСІЁЃ
гыL.crispatusВЛЭЌЃЌL.inersЕФЩњГЄвРРЕгкАыызАБЫсЃЛАыызАБЫсвжжЦМСгыМзЯѕпђСЊгУЃЌдкЬхЭтЭЈЙ§ПЩвжжЦL.inersЃЌВЂДйНјL.crispatusЕФЗсЖШЁЃгУзюМбОњжжНјааВЙГфжЮСЦЃЌЛђАаЯђжЮСЦетаЉЗЧзюМбЯИОњЃЌПЩФмгажњгкМѕЩйЯИОњадвѕЕРбзИДЗЂЕФИХТЪЁЃ
▸ еыЖдВЛЭЌЕФвѕЕРЮЂЩњЮязщГЩгУвЉвВВЛЭЌ
1.ШщЫсИЫОњВПЗжаЏДј (>5%)
ПкЗўЛђОжВПЪЙгУМзЯѕпђЛђЬцЯѕпђЃЌвђЮЊШщИЫОњЖдМзЯѕпђЁЂЬцЯѕпђВЛУєИаЃЌЧвФмЩБУ№ЦфЫћбсбѕОњЁЃ
2.ШщЫсИЫОњМИКѕВЛаЏДј (<1%)ЃЌбсбѕаЭ
ПкЗўЛђОжВПЪЙгУМзЯѕпђЛђЬцЯѕпђЛђПЫСжУЙЫиЃЌвђЮЊ
МзЯѕпђЁЂЬцЯѕпђВЛУєИаЃЌЧвФмЩБУ№ЦфЫћбсбѕОњЁЃ
3.ШщЫсИЫОњМИКѕВЛаЏДј (<1%)ЃЌашбѕаЭ
ПкЗўЛђОжВППЫСжУЙЫиЛђПЈФЧУЙЫиЮЊжїЃЌвђЮЊПЫСжУЙЫиЖджївЊЕФКУбѕОњУєИаЁЃ
▸ вѕЕРЮЂЩњЮявЦжВ
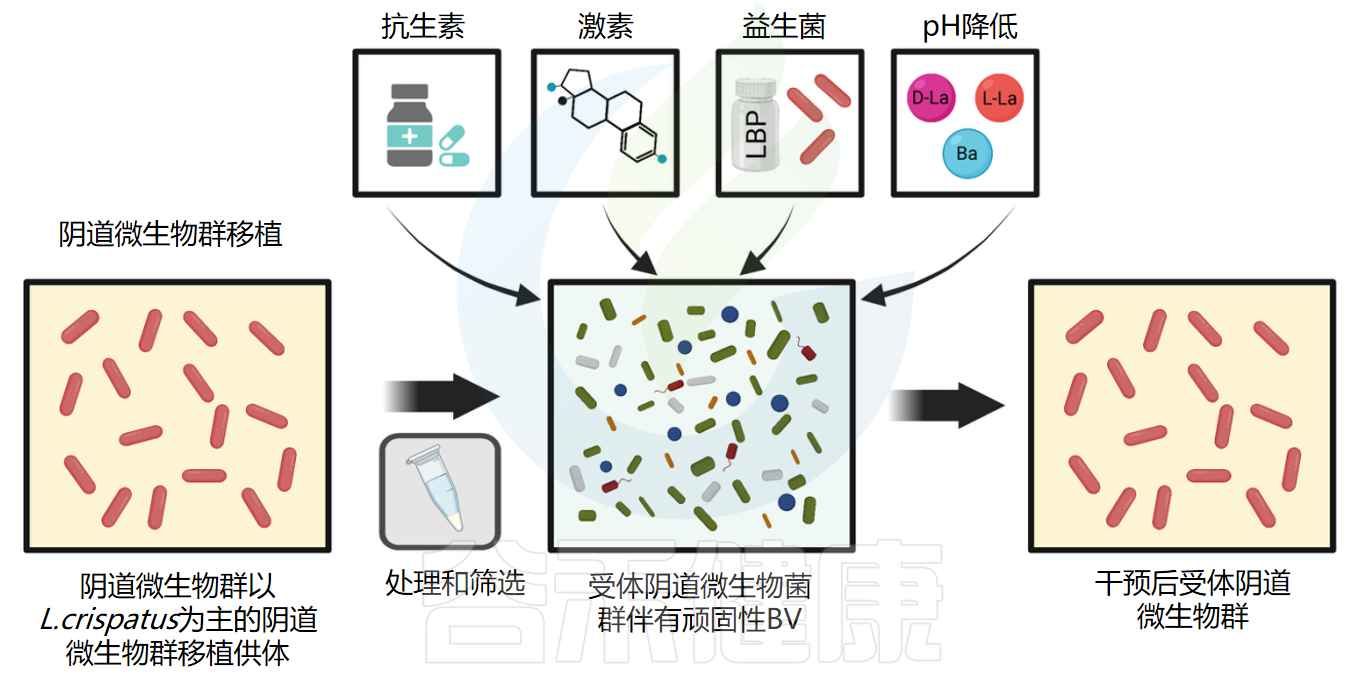
France M,et al.Nat Microbiol.2022
ЯжгаЕФжЮСЦЗНЗЈАќРЈМзЯѕпђЕШПЙЩњЫиЁЂДЦМЄЫиСЦЗЈЁЂШщЫсКЭХ№ЫсвдМАвѕЕРШщЫсИЫОњвцЩњОњЁЃШЛЖјЃЌетаЉИЩдЄДыЪЉЕФГЩЙІТЪИїВЛЯрЭЌЃЌВЂЧвВЛФмгааЇдЄЗРИДЗЂад/ЭчЙЬад BVЁЃ
вѕЕРЮЂЩњЮявЦжВ (VMT) ЪЧжЮСЦBVЕФвЛжжгаЧАОАЕФИЩдЄДыЪЉЁЃШЗЖЈСЫОпгаШщИЫОњгХЪЦвѕЕРЮЂЩњЮяШКЕФКЯЪЪЙЉЬхЁЃДгОшдљепДІЪеМЏвѕЕРЗжУкЮяЃЌЩИВщИїжжадДЋВЅИаШОВЂНјааДІРэЁЃШЛКѓНЋДІРэКѓЕФвѕЕРЗжУкЮяв§ШыЭЈГЃЛМгаИДЗЂад/ЭчЙЬад BV ЕФНгЪмепЕФвѕЕРжаЁЃНгЪмепдквЦжВЧАПЩФмЛсЛђПЩФмВЛЛсНгЪмПЙЩњЫижЮСЦЁЃГЩЙІЕФЖЈвхЪЧЪмЬхЯИОњадвѕЕРбзЕФГжОУНтОівдМАЦфвѕЕРЮЂЩњЮяШКЯђШщИЫОњеМжїЕМЕиЮЛЕФзЊБфЁЃ
НсгявѕЕРЮЂЩњЮяШКЕФЦНКтЖдХЎадНЁПЕжСЙиживЊЁЃвђДЫЃЌвѕЕРОњШКМьВтдкЦРЙРХЎадНЁПЕзДПіЗНУцОпгаживЊвтвхЁЃЭЈЙ§МьВтвѕЕРЮЂЩњЮяШКЕФзщГЩЃЌПЩвдМАдчЗЂЯжЧБдкЕФЮЪЬтЃЌВЂВЩШЁЯргІЕФИЩдЄДыЪЉЃЌвдИФЩЦХЎадЕФЩњжГНЁПЕКЭШбЩяГЩЙІТЪЁЃетВЛНігажњгкЬсИпИЈжњЩњжГММЪѕЕФаЇЙћЃЌЛЙПЩвдНЕЕЭдчВњЁЂаТЩњЖљВЂЗЂжЂЕШВЛСМШбЩяНсОжЕФЗчЯеЃЌЖдгкгХЛЏХЎадНЁПЕЙмРэКЭОпгаживЊвтвхЁЃ
жївЊВЮПМЮФЯз
Gupta S, Kakkar V, Bhushan I. Crosstalk between Vaginal Microbiome and Female Health: A review. Microb Pathog. 2019 Nov;136:103696.
France M, Alizadeh M, Brown S, Ma B, Ravel J. Towards a deeper understanding of the vaginal microbiota. Nat Microbiol. 2022 Mar;7(3):367-378.
Chee WJY, Chew SY, Than LTL. Vaginal microbiota and the potential of Lactobacillus derivatives in maintaining vaginal health. Microb Cell Fact. 2020 Nov 7;19(1):203.
Shen L, Zhang W, Yuan Y, Zhu W, Shang A. Vaginal microecological characteristics of women in different physiological and pathological period. Front Cell Infect Microbiol. 2022 Jul 22;12:959793.
Chen X, Lu Y, Chen T, Li R. The Female Vaginal Microbiome in Health and Bacterial Vaginosis. Front Cell Infect Microbiol. 2021 Apr 7;11:631972.
Bayar E, Bennett PR, Chan D, Sykes L, MacIntyre DA. The pregnancy microbiome and preterm birth. Semin Immunopathol. 2020 Aug;42(4):487-499.
Chen T, Wu R, Cheng L, Liao Q, Chen Z. Editorial: Vaginal microecological disorder and gynecological diseases. Front Cell Infect Microbiol. 2023 Oct 18;13:1292815.
Gu Y, Zhou G, Zhou F, Li Y, Wu Q, He H, Zhang Y, Ma C, Ding J, Hua K. Gut and Vaginal Microbiomes in PCOS: Implications for Women's Health. Front Endocrinol (Lausanne). 2022 Feb 23;13:808508.
Kalia N, Singh J, Kaur M. Microbiota in vaginal health and pathogenesis of recurrent vulvovaginal infections: a critical review. Ann Clin Microbiol Antimicrob. 2020 Jan 28;19(1):5.
Han Y, Liu Z, Chen T. Role of Vaginal Microbiota Dysbiosis in Gynecological Diseases and the Potential Interventions. Front Microbiol. 2021 Jun 18;12:643422.
Fettweis JM, Serrano MG, Brooks JP, Edwards DJ, Girerd PH, Parikh HI, Huang B, Arodz TJ, Edupuganti L, Glascock AL, Xu J, Jimenez NR, Vivadelli SC, Fong SS, Sheth NU, Jean S, Lee V, Bokhari YA, Lara AM, Mistry SD, Duckworth RA 3rd, Bradley SP, Koparde VN, Orenda XV, Milton SH, Rozycki SK, Matveyev AV, Wright ML, Huzurbazar SV, Jackson EM, Smirnova E, Korlach J, Tsai YC, Dickinson MR, Brooks JL, Drake JI, Chaffin DO, Sexton AL, Gravett MG, Rubens CE, Wijesooriya NR, Hendricks-Muñoz KD, Jefferson KK, Strauss JF 3rd, Buck GA. The vaginal microbiome and preterm birth. Nat Med. 2019 Jun;25(6):1012-1021.
БОЮФзЊздЃКЙШКЬНЁПЕ
https://m.sciencenet.cn/blog-2040048-1434234.html
ЩЯвЛЦЊЃК[зЊди]ГІЕРВЁдЬхИаШОЖЈжВЕФШ§ИіЙиМќНЧЩЋЁЊЁЊбзжЂЁЂгЊбјгыЙВЩњОњШК
ЯТвЛЦЊЃК[зЊди]УтвпЗРгљКЭДњаЛПижЦЪЎзжТЗПкЕФбзадаЁЬх