博文
阿伦尼乌斯方程微分式的应用
|
1889年瑞典人阿伦尼乌斯(Arrhenius)提出了著名的阿伦尼乌斯方程指数式[1],揭示了温度对化学速率常数的影响规律,参见如下式(1):
(1)
本文拟结合具体实例,介绍阿伦尼乌斯方程微分式在化学动力学中的应用技巧,供参考.
阿伦尼乌斯方程微分式
由式(1)可得:
(2)
设一定温度范围内,指前因子A及活化能Ea均与温度无关,则式(2)对温度求导可得:
(3)
式(3)称阿伦尼乌斯方程微分式.
阿伦尼乌斯方程微分式的应用
[例1] 反应H2+I2=2HI的机理可能为[2]:
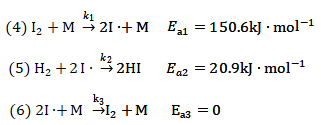
试推导该反应的速率方程,并计算其表观活化能.
解:Ⅰ反应速率方程推导
依据质量作用定律,由式(4)可得:
dc(I·)/dt=2k1·c(I2)·c(M) (7)
同理由式(5)可得:dc(I·)/dt=-2k2·c(H2)·c2(I·) (8)
由式(6)可得:dc(I·)/dt=-2k3·c(M)·c2(I·) (9)
式(7)、(8)及(9)结合稳态法可得:
dc(I·)/dt=2k1·c(I2)·c(M)-2k2·c(H2)·c2(I·)-2k3·c(M)·c2(I·)=0 (10)
整理式(10)可得:
c2(I·)=k1·c(I2)·c(M)/[k2·c(H2)+k3·c(M)] (11)
依题:Ea3=0, 则:k3·c(M)>>k2·c(H2),此时式(11)可化简为:
c2(I·)=(k1/k3)·c(I2) (12)
另由式(6)可得:dc(HI)/dt=2k2·c(H2)·c2(I·) (13)
将式(12)代入式(13)可得:
dc(HI)/dt=(2k1·k2/k3)·c(H2)·c(I2) (14)
Ⅱ 表观活化能的计算
设总反应的速率常数为k,表观活化能为Ea.
由式(14)可得:k=2k1·k2/k3 (15)
由式(15)可得:
(16)
将式(3)代入式(16)可得:
(17)
式(17)两边同乘RT2可得:Ea=Ea1+Ea2-Ea3=150.6kJ·mol-1+20.9kJ·mol-1=171.5kJ·mol-1
[例2]反应物A,按平行反应方式同时得到B、C产物,参见如下图1.

设平行反应及反应1、2均为一级反应,反应1、2的活化能分别为Ea1和Ea2,计算平行反应的总表观活化能Ea.
解:依题 v=k·c(A)=k1·c(A)+k2·c(A)=(k1+k2)·c(A) (18)
由式(18)可得:k=k1+k2 (19)
由微积分原理可得:dlnk=dk/k (20)
将式(20)代入式(3)可得:dlnk/dT=dk/(k·dT)=Ea/(RT2) (21)
整理上式可得:dk/dT=k· Ea/(RT2) (22)
同理可得:dk1/dT=k1· Ea1/(RT2) (23)
dk2/dT=k2· Ea2/(RT2) (24)
又因为: dk/dT=d(k1+k2)/dT=dk1/dT+dk2/dT (25)
将式(22)、(23)及(24)依次代入式(25)可得:
k· Ea/(RT2)=k1· Ea1/(RT2)+k2· Ea2/(RT2) (26)
式(26)两边同乘RT2可得:
k·Ea=k1·Ea1+k2·Ea2 (27)
则:Ea=(k1·Ea1+k2·Ea2)/(k1+k2)
3. 结论
阿伦尼乌斯方程微分式与微积分原理结合, 可灵活应用于动力学表观活化能的计算.
参考文献
[1]Laidler J K. The development of the Arrhenius equation. Journal of chemical education, 1984, 61(6):494
[2]天津大学物理化学教研室编.物理化学(第五版,下册).北京:高等教育出版社,2009,5:610
https://m.sciencenet.cn/blog-3474471-1371592.html
上一篇:平衡态热力学与准静态过程假说熵变的计算结果类比(Ⅱ)
下一篇:(PbO2/PbSO4)标准电极电势的热力学计算