博文
[转载]综述:铁死亡的最新诱导剂和抑制剂
||
https://zhuanlan.zhihu.com/p/597711297
关注“Being科学”微信公众号
铁死亡是一种新的铁依赖细胞程序性死亡形式,其特征是铁积累和脂质过氧化。近年来,由于铁死亡与许多疾病的病理生理过程密切相关,铁死亡引起了研究界的极大兴趣。最近的研究显示了一些关键靶点,如谷胱甘肽过氧化物酶4(GPX4)和System Xc−,已经开发了几种诱导剂和抑制剂来调节这些关键靶点。随着新的脱铁靶点的出现,诱导剂和抑制剂的研究取得了新的进展。诱导剂和抑制剂的选择和使用对相关工作非常重要。
近日,杂志《cell death discovery》上刊登了一篇题为“Recent progress in ferroptosis: inducers and inhibitors” 的报道。该综述简要介绍了铁死亡代谢途径中的重要调控靶点,列出并分类了常用的和最近开发的铁死亡诱导剂和抑制剂,并讨论了它们的医学应用。

诱导剂
1)针对铁代谢的小分子和药物诱导剂
Erastin是于2003年首次被发现一种基因选择型抗肿瘤剂。Erastin以多种方式诱导铁死亡,其中一种是针对VDAC。VDAC有三种异构体,VDAC2和VDAC3的敲除会导致相关细胞对Erastin的耐药性。然后,Erastin将通过直接与VDAC2结合来诱导脂质ROS的产生。除了Erastin,RSL5是另一种具有类似效果的化合物,能够与VDAC3结合诱导铁死亡。此外,VDACs可以被另一个名为4,4′-二异硫氰基硫烯基苯-2,2′-二磺酸(DIDS)的线粒体阴离子通道的小型分子变构阻滞剂抑制。阻断VDAC会增加细胞对电离辐射的敏感性,并抑制DNA损伤的修复。因此,DIDS已被证明可以提高放射治疗癌症的疗效。细胞中的铁水平是另一个重要指标。二价金属转运体1(DMT1)与细胞内铁和铁稳态水平有关。最近的一项研究表明,替莫唑胺(TMZ)是一种治疗胶质母细胞瘤的抗肿瘤药物,可以通过增强DMT1诱导铁死亡。另一个名为MMRi62的小分子是最近发现的诱导剂,据报道它诱导了铁蛋白重链的降解。
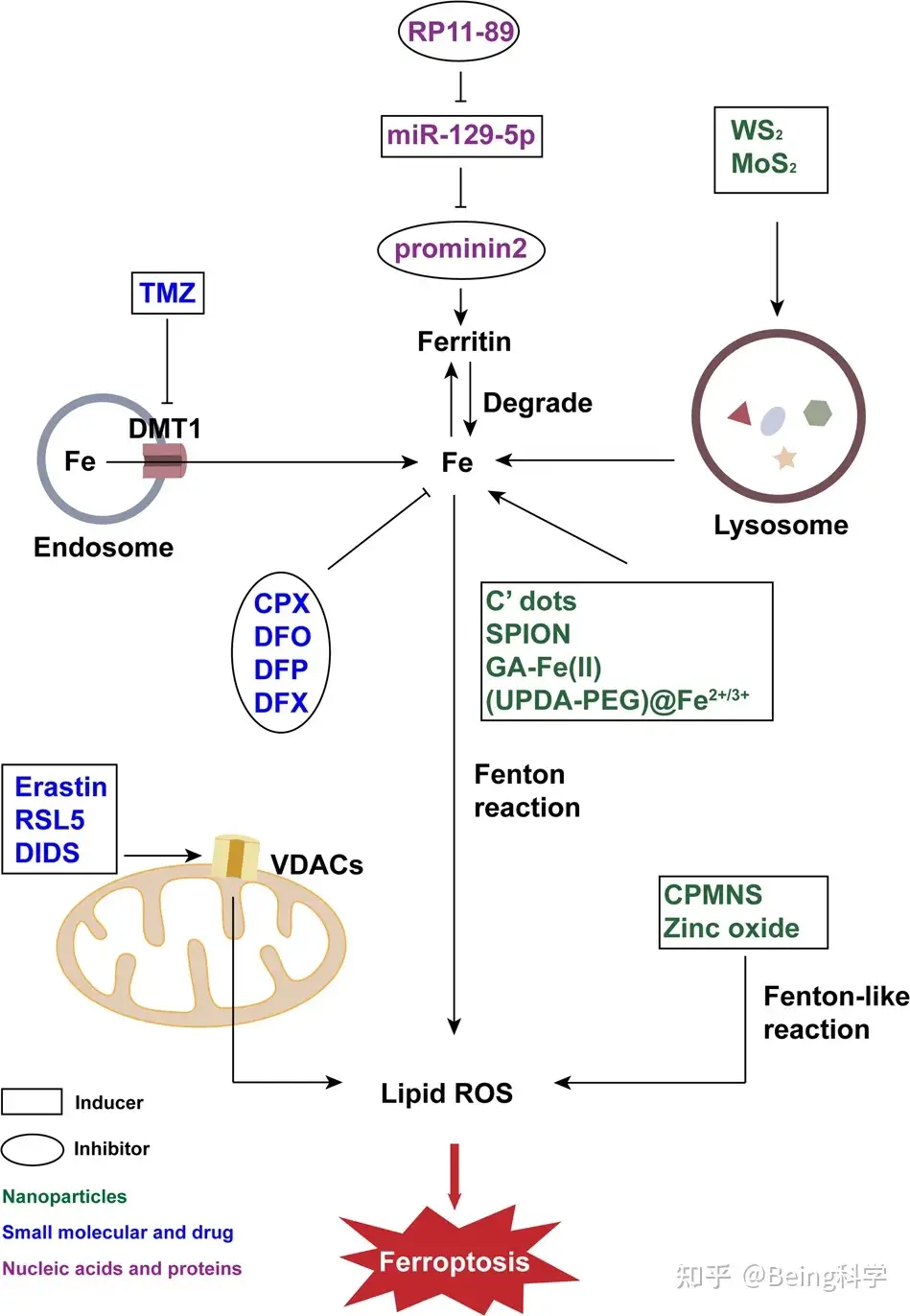
2)针对脂质代谢的小分子和药物诱导剂
铁死亡也可以通过影响脂质代谢和直接产生脂质ROS来诱导。在治疗肝癌方面,FDA认证的抗肿瘤药物索拉非尼可以在ACSL4存在的情况下诱导铁死亡。特别是索拉非尼的添加直接影响了细胞中脂质ROS生成的代谢途径。另一个直接影响脂质ROS水平的诱导剂是三级-丁基过氧化氢(t-BuOOH),在给药时可能会导致氧化应激、线粒体膜电位异常和DNA损伤。然而,线粒体膜电位的塌陷不是细胞死亡的根本原因。作为最近报道的铁死亡诱导剂,t-BuOOH通过心脂的氧化发挥作用,心脂蛋白氧化的抑制剂(如XJB-5-131和JP4-039)可以起到逆转作用。
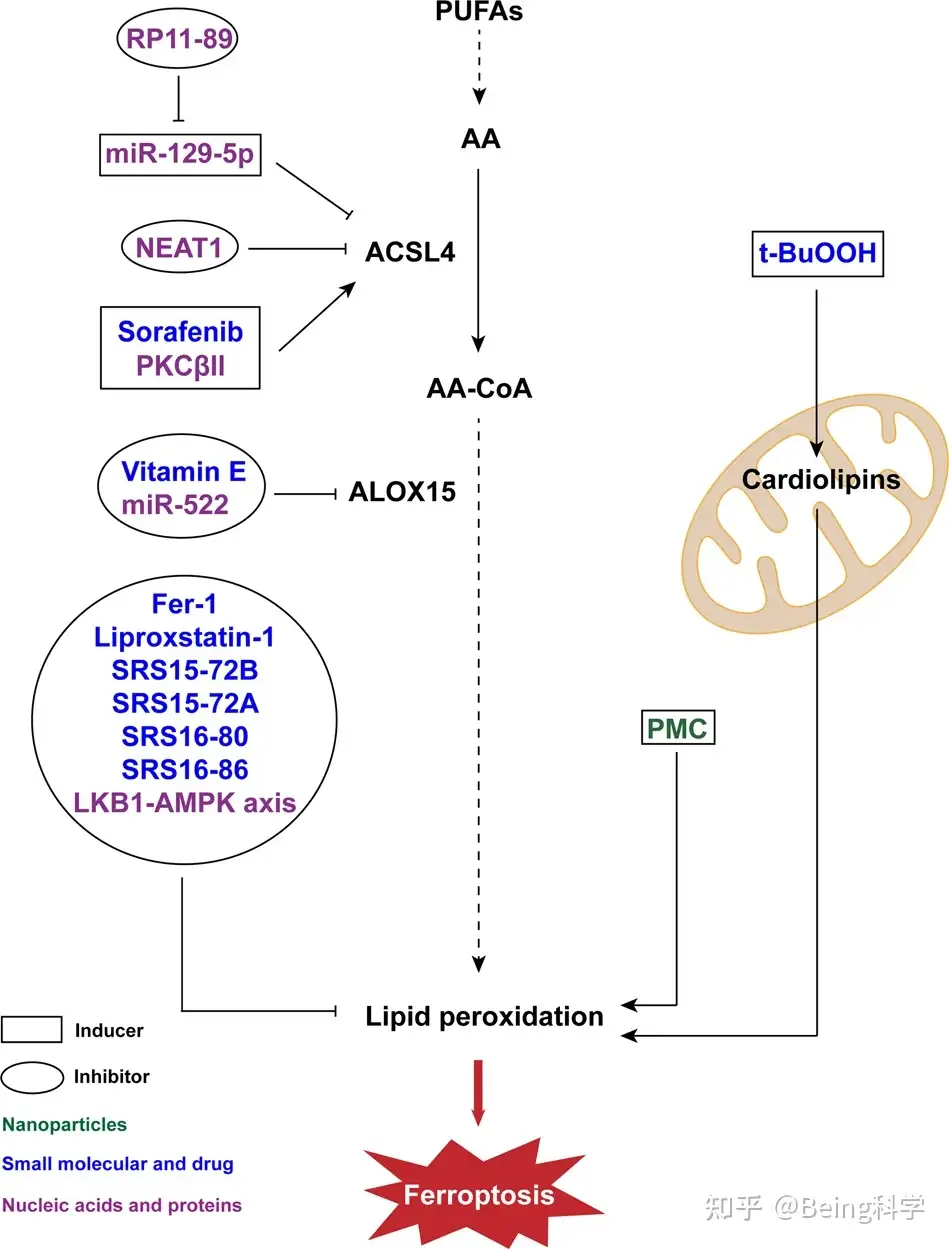
3)针对GSH/GPX4轴的小分子和药物诱导剂
GSH的生产和氧化过程有多个可以调节的环节。RSL3与RSL5一起被发现,尽管它们的功能不同。RSL3针对具有亲核活性位点的酶,作用于GPX4诱导铁死亡。其他化合物,如ML162、DPI7和DPI10,具有类似于RSL3的作用。此外,另一种名为FIN56的化合物可以促进GPX4的降解。GCL是参与生产GSH的重要酶,其抑制会导致铁死亡。除了阻断VDAC外,Erastin还影响GSH的形成和氧化过程。System L是一种氨基酸转运体,与System Xc−不同,由SLC7A5和SLC3A2组成。Erastin与SLC7A5相结合,导致System L的活动减少。这个过程不会直接诱导铁死亡,但它会影响System Xc−的活力和细胞的胱氨酸摄入。
此外,Erastin可能会耗尽GSH并导致GPX4的降解。Erastin的一些类似物,如MEII、PE和AE也具有类似的功能。与不会导致细胞死亡的类似物相比,它们对GSH的消耗有更好的影响。这些类似物是否可以结合VDAC并抑制System Xc−需要进一步研究,但众所周知,它们的效果是通过消耗GSH实现的。除了Erastin及其类似物外,已知还有多种药物可以阻断System Xc−。经FDA认证的磺胺沙拉嗪(SAS)抑制System Xc−并表现出抗肿瘤作用。Sorafenib通过阻断其上游调节器间接阻断System Xc−,并间接抑制GPX4。

4)针对FSP1/CoQ相关途径的小分子和药物诱导剂
NDP4928是一种小分子,与其说是诱导剂,不如说是铁死亡的增强剂。据报道,NDP4928单独表现出弱细胞毒性,但与RSL3治疗时,其细胞毒性可能会大大增强。此外,当与BSO共同治疗时,NDP4928的细胞毒性也得到了增强。众所周知,FSP1是NDP4928的靶标,这种化合物结合和抑制FSP1,以增强GSH抑制引起的铁死亡。除了Erastin外,FIN56是另一种具有多种效果的诱导剂。FIN56不仅通过GPX4的降解,还通过与角鲨烯合成酶(SQS)结合和耗尽CoQ诱导铁死亡。他汀类药物被广泛用于治疗许多疾病。其中一些已经获得了FDA的认证。他汀类药物已被配制为治疗性纳米颗粒,在甲烷酸盐途径中阻断3-羟基-3-甲基谷氨基-CoA还原酶(HMGCR)。随着CoQ的减少,随后发生了铁死亡。
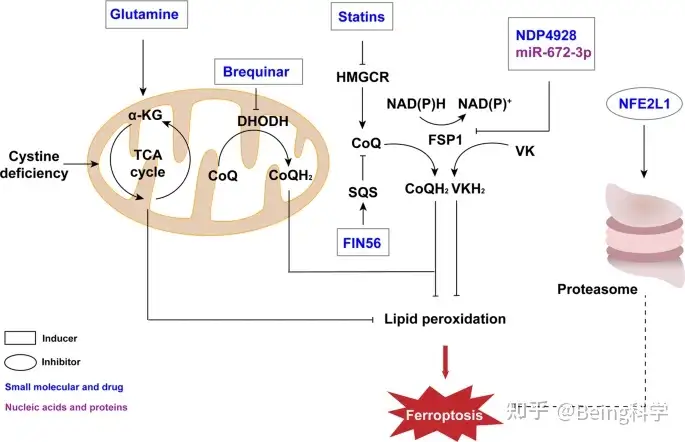
5)针对其他途径的小分子和药物诱导剂
虽然大多数铁死亡的诱导通过上述三种方式工作,但也有一些诱导因素通过影响其他靶点。例如,DHODH可以通过brequinar抑制。因此,brequinar可以通过诱导肿瘤细胞中的铁死亡来抑制肿瘤生长。广泛使用的药物地塞米松通过上调称为二肽酶-1(DPEP1)的GSH代谢途径的调节剂来增加细胞对铁死亡的敏感性。一些具有特殊结构和功能的纳米颗粒可以诱导铁死亡。这些纳米颗粒具有共性,可能导致铁水平或ROS水平的变化。非编码RNA,包括微RNA,在多个细胞过程中发挥调节作用,并调节具有多个目标的铁沉着作用。
抑制剂
1)降低铁水平的小分子抑制剂
消除过多的铁离子是抑制铁死亡的直接方法。据报道,ciclopirox olamine(CPX)是一种铁螯合剂,也具有广谱抗真菌和抗菌能力。除了通过螯合铁离子抑制铁死亡,CPX-O已被证明可以诱导多囊肾病小鼠铁蛋白降解。去氧胺(DFO)是另一种广泛使用的铁螯合剂。据报道,它被用来抑制铁死亡,对创伤性脊髓损伤有治疗作用。除了CPX和DFO外,还报告了许多其他铁螯合剂,如deferiprone(DFP)和deferasirox(DFX)。
2)用于减少过氧化脂的小分子抑制剂
2012年,铁抑素-1(Fer-1)确定为铁死亡抑制剂,Fer-1能抑制HT-1080细胞中的RSL3或Erastin诱导的铁血病。研究证明,Fer-1通过抑制脂质过氧化发挥作用。此外,Fer-1可以挽救由过度活跃的p53引起的铁死亡。在铁死亡的调节中,p53是一种调节System Xc−的重要蛋白质,可以通过在激活时诱导铁死亡来促进胚胎致死性。除了抑制RSL3或Erastin诱导的铁死亡外,有研究表明,Fer-1可以提高GSH水平,以抑制细胞的铁死亡。另一种常用的有效脂质抗氧化剂是脂质抑素-1。在没有GPX4的情况下,它可以保护细胞免受铁死亡的侵害。此外,ɑ-生育酚(维生素E)和Fer-1的类似物,如SRS15-72B、SRS15-72A、SRS16-80和SRS16-86也具有相似的功能,尽管效果和稳定性不同。最近的研究表明,维生素K(VK)可以转化为相应的对苯二酚(VKH2),FSP1可以催化这一过程。VKH2是VK的完全还原形式,具有抑制脂质氧化的能力,并具有抑制铁死亡作用。
3)影响GSH/GPX4轴的小分子抑制剂
众所周知,当System Xc−在帮助细胞吸收胱氨酸的过程中被阻塞时,β-巯基乙醇(β-ME)会抑制铁死亡。在这个过程中,β-ME与胱氨酸反应并形成混合二硫化物。混合二硫化物通过System L转移到细胞中,并迅速产生胱氨酸。增加GPX4的表达反过来可以抑制铁死亡。硒(Se)可以通过激活转录因子TFAP2c(转录因子激活蛋白2γ)和Sp1(特异性蛋白1)来调节这个过程。此外,据报道GPX4水平低的细胞无法受到Se的保护。2-氨基-5-氯-N,3-二甲基苯甲酰胺(CDDO)是一种三萜化合物,可抑制分子伴侣热休克蛋白90(HSP90)。CDDO已被证明可以抑制GPX4降解并保护细胞免受铁死亡的影响。
4)具有抑制作用的核酸和蛋白质
一些蛋白质也参与铁的代谢,例如prominin2可以促进多囊泡体和外切体的形成。铁蛋白从prominin2控制的细胞中分泌,从而增加铁死亡耐药性。有许多具有抑制作用的非编码RNA,如LINC00336。RP11-89是一种长链的非编码RNA,通过调节miR-129-5p来抑制铁死亡。此外,miR-522通过另一种名为arachidonate lipoxygenase 15(ALOX15)的酶抑制铁死亡。
LKB1(肝激酶B1)-AMPK(AMP激活蛋白激酶)轴通过调节乙酰辅酶A羧化酶1(ACC1)的活性来调节铁死亡。事实证明,ACC1催化脂肪酸的生物合成。作为AMPK的下游底物,当AMPK被铁死亡相关的信号激活时,ACC1会磷酸化并受到抑制。M1肿瘤相关巨噬细胞有另一种代谢途径,可以抑制脂质ROS的产生,在没有GPX4的情况下,比M2亚型对铁死亡更不敏感。M1亚型细胞表达诱导一氧化氮(NO)合成酶(iNOS)并产生NO。NO可以消除脂质过氧化,并保护M1亚型细胞免受铁死亡。
Dickkopf-1(DKK1)可以抑制Wnt/β-catenin途径并促进肿瘤发育。最近,DKK1被确定为具有铁死亡抑制作用。DKK1保护肿瘤细胞免受铁死亡的影响,对于转移性生长是必不可少的。DKK1的抑制作用是通过增加SLC7A11的表达来实现的,SLC7A11是System Xc−的一个亚基。由于DKK1可以抑制Wnt/β-catenin通路,它间接降低了信号传感器和转录3(STAT3)激活剂的活性,从而与SLC7A11的启动子区域结合并抑制其表达。此外,SLC7A11可以通过脱双喹酶OTUB1稳定。OTUB1在人类肿瘤细胞中高度表达,因此可以防止铁死亡。
多种疾病可以用铁死亡诱导剂或抑制剂治疗。铁死亡已被应用于肿瘤、神经疾病、器官损伤等的治疗。许多研究都提供了证据证明铁死亡可以抑制肿瘤生长。铁死亡诱导剂已被证明对体内和体外的多个肿瘤细胞具有细胞毒性。由于铁死亡可以由一些纳米颗粒诱导,因此修改这些纳米颗粒是诱导肿瘤组织中铁死亡的另一种有效方法。
一些神经系统疾病也与铁死亡有关。最近的一项研究表明,一种名为载脂蛋白E(ApoE)的脂质转运糖蛋白是阿尔茨海默病的主要蛋白质,它能够保护细胞免受各种铁死亡诱导剂的侵害。ApoE通过激活PI3K/AKT途径来减少铁蛋白的铁释放来抑制铁死亡。此外,在阿尔茨海默氏症的小鼠模型中,铁死亡导致神经元死亡和记忆障碍,这些症状可以通过铁死亡抑制剂改善。脑出血是中风的一个亚型,也与铁死亡有关。阻断铁死亡对脑出血以及其他一些神经疾病的发生和进展有治疗作用。
除了癌症和神经系统疾病外,结核病和自身免疫性疾病也可能受到铁死亡的调节。结核病是由结核分枝杆菌(Mtb)引起的。Mtb感染导致宿主细胞坏死,铁死亡被证明是所涉及的机制之一。最近的一项研究表明,系统性红斑狼疮患者的中性粒细胞患有铁死亡。在患者的中性粒细胞中,GPX4的表达被抑制。
综上所述,铁死亡是一种程序性细胞死亡形式,具有很高的应用前景,但仍然需要进一步研究。诱导剂和抑制剂的开发对于铁死亡的研究至关重要。不断发现新的铁死亡目标和机制,可以为各种类型的疾病提供新的治疗药物和方法。
https://m.sciencenet.cn/blog-40692-1417274.html
上一篇:[转载]拥有良好的社交和友谊会使肠道微生物群更健康
下一篇:[转载]SK channel-mediated metabolic escape to glycolysis inhibits
