博文
还原半反应的标准摩尔吉布斯自由能变与元素电势图
|
本文拟讨论还原半反应的标准摩尔吉布斯自由能变[1](ΔhGθm)在元素电势图中的不可替代作用.
1. 还原半反应的标准摩尔吉布斯自由能变
还原半反应的标准摩尔吉布斯自由能变是联系不同还原半反应的重要的纽带, 也是元素电势图计算的理论基石.
还原半反应通式为:氧化型+ze- = 还原型
其标准电极电势记为Eθ(氧化型/还原型),则还原半反应的标准摩尔吉布斯自由能变为:
ΔhGθm=-zFEθ(氧化型/还原型)
2. 元素电势图
将同一元素不同氧化值的物质按氧化值由高到底顺序排列,相邻两种氧化数物质用短线段连接,并标出对应电对的标准电极电势, 该类图形称元素的标准电极电势图,简称元素电势图.
元素电势图实例参见图1及图2[2].
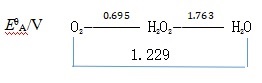

图1 酸性介质中氧元素的标准电极电势图 图2 碱性介质中氧元素的标准电极电势图
图1、2分别表示酸性及碱性介质中氧元素的标准电极电势图.
由图1可获取的直接信息包括c(H+)=1.0mol·dm-3时Eθ(O2/H2O2)=0.695V;Eθ(H2O2/H2O)=1.763V及
Eθ(O2/H2O)=1.229V.
同理由图2可获取的直接信息包括c(OH-)=1.0mol·dm-3时Eθ(O2/HO2-)=-0.076V;Eθ(HO2-/OH-)=0.867V 及
Eθ(O2/OH-)=0.401V.
3. 元素电势图的计算
例1.现有如下元素电势图(参见图3):
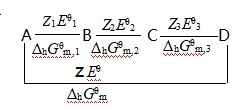
图3 元素的标准电极电势图
则:ΔhGθm,1=-z1F·Eθ1 (1)
ΔhGθm,2=-z2F·Eθ2 (2)
ΔhGθm,3=-z3F·Eθ3 (3)
ΔhGθm=-zF·Eθ (4)
z=z1+z2+z3 (5)
ΔhGθm=ΔhGθm,1+ΔhGθm,2+ΔhGθm,3 (6)
将 式(1)、(2)、(3)、(4)及(5)分别代入式(6)整理可得:
Eθ(A/D)=(z1Eθ1+z2Eθ2+z3Eθ3)/(z1+z2+z3) (7)
式(7)即为元素电势图计算电极电势公式.
4. 歧化反应判据
下面讨论用元素电势图判定在标准状态下歧化反应自发性判据.
例:已知酸性介质中铜的元素电势图如下(参见图4):

图4 铜元素的标准电极电势图
试判定标准状态下Cu+发生歧化反应的自发性.
解:酸性介质中Cu+歧化反应为 2Cu+ = Cu + Cu2+
可依据歧化反应设计原电池如下:Pt∣Cu+(α=1), Cu2+(α=1)║Cu+(α=1)▏Cu
阴极:Cu+(α=1)+e- = Cu
阳极:Cu+(α=1)=Cu2+(α=1)+e-
原电池电动势:Eθ=Eθ+ - Eθ- =Eθ(右)- Eθ(左)=0.520-0.159=0.361V>0
表明标准状态下Cu+歧化反应自发.
由上可得标准状态下,歧化反应自发性判据为Eθ(右)> Eθ(左).
5. 结论
⑴ ΔhGθm=-zFEθ(氧化型/还原型);
⑵Eθ(A/D)=(z1Eθ1+z2Eθ2+z3Eθ3)/(z1+z2+z3);
⑶标准状态下,歧化反应自发性判据为元素电势图中Eθ(右)> Eθ(左).
参考文献
[1]余高奇,陈阳,李凤莲. 还原半反应相关热力学计算. 大学化学, 2013,28(3):61-66
[2]天津大学无机化学教研室编; 王建辉等修订. 第五版. 北京:高等教育出版社,2018,6:94,96.
https://m.sciencenet.cn/blog-3474471-1337700.html
上一篇:一道电化学题目解析
下一篇:铬的理化性质、水解及重要工业产品制备介绍