博文
偏摩尔量的热力学定义合理性探究
|
本文拟结合具体实例探讨热力学偏摩尔量定义的合理性,供参考.
偏摩尔量
偏摩尔量是指均相多组分系统中,单位物质的量的B组分所拥有的具有容量性质的某状态函数(诸如U、
H、G、A、S或V等).
例如:水与乙醇形成的均相二组分系统,水与乙醇的偏摩尔体积V(H2O)和V(C2H5OH)参见如下图1.
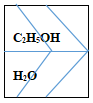
图1. 水-乙醇二组分系统示意图
在一定温度、压强及组成前提下,水与乙醇的偏摩尔体积V(H2O)和V(C2H5OH)满足如下式(1):
V=n(H2O)·V(H2O)+n(C2H5OH)·V(C2H5OH) (1)
式(1)中“V”代表系统总体积;“n(H2O)、n(C2H5OH)”分别表示系统中水与乙醇的物质的量.
式(1)中“n(H2O)、n(C2H5OH)”是配制溶液时的可控制量;“V”是可测量;“V(H2O)和
V(C2H5OH)”是物理手段不可测量.
由于存在两个未知量,因此从纯物理或数学角度分析,由式(1)不可能获取水与乙醇的偏摩尔体积.
另需指出仅当系统状态确定后,偏摩尔体积才有明确的物理意义;状态改变,偏摩尔体积一定发生改变.
2.偏摩尔量的热力学定义
平衡态热力学认为:在温度、压强及组成恒定前提下,改变nB所引起的具有广度性质的状态函数X的变化
率,称为组分B的偏摩尔量XB;记为:
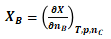 (2)
(2)
式(2)中“nC”代表除B以外的其余组分的物质的量.
为了保证式(2)中组成恒定,平衡态热力学指定了偏摩尔量XB的定义式应用的两种特定情况.
①在一个足够大的具有一定组成的均相多组分系统,加入单位物质的量的B组分,所引起系统广度性质X的
增量;
②在一个具有一定组成的均相多组分系统,加入B组分微小改变量dnB,所引起系统广度性质X的变化率;
上述两种情况下,加入B组分,系统的组成均可保持恒定; 这也是偏摩尔量热力学定义的核心之一.
通常上述两种情况很难客观实现;因此偏摩尔量的式(2)定义只具有理论意义.
3.偏摩尔体积的测定
现阶段物化教科书获取均相多组分中物质的偏摩尔体积的方法,参见如下[例1].
[例1]. 298.15K和100kPa下,在1.0kg的H2O(A)中加入NaBr(B),所得溶液体积与溶质B的质量摩尔浓
度mB之间关系为[1]:
V/cm3=1002.93+23.189(mB/mol·kg-1)+2.197(mB/mol·kg-1)3/2-0.178(mB/mol·kg-1)2 (3)
试计算mB=0.25mol·kg-1时,H2O(A)与NaBr(B)的偏摩尔体积.
解:1kgH2O(A)中,NaBr的mB即为nB.
 (4)
(4)
将式(3)代入式(4),并整理可得:
VNaBr/(cm3·mol-1)=23.189+3.296(mB/mol·kg-1)1/2-0.356(mB/mol·kg-1) (5)
将mB=0.25mol·kg-1分别代入式(3)和(5)可得:
V/cm3=1008.991 (6)
VNaBr/(cm3·mol-1)=24.748 (7)
另1kg水,nH2O=1000g/(18.016g·mol-1)=55.556mol;nNaBr=0.25mol
由偏摩尔量集合公式可得:V=nH2O·VH2O+nNaBr·VNaBr (8)
将水与NaBr的摩尔数与式(6)、(7)数据依次代入式(8),可解得:
VH2O=18.050cm3·mol-1 (9)
需明确实际测量过程,加入NaBr(B)后,尽管H2O(A,1kg)的质量未变,混合溶液中H2O(A,1kg)与NaBr(B)
的组成一定改变;此时由式(4)计算得到并不是严格意义的NaBr偏摩尔体积,它仅为一种数学拟合.
4.结论
⑴从纯物理或数学角度分析,偏摩尔体积的绝对值不可能获取;
⑵组成恒定是偏摩尔量定义的前提;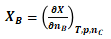 只具有理论意义.
只具有理论意义.
⑶现阶段物化教科书获取的偏摩尔体积,仅为一种数学拟合.
参考文献
[1]沈文霞.物理化学核心教程(第二版).北京:科学出版社,2009:117
https://m.sciencenet.cn/blog-3474471-1406117.html
上一篇:浅析国内物化教科书可逆过程阐释的困惑
下一篇:可逆电池的新解读