博文
组蛋白甲基化 - MedChemExpress
|
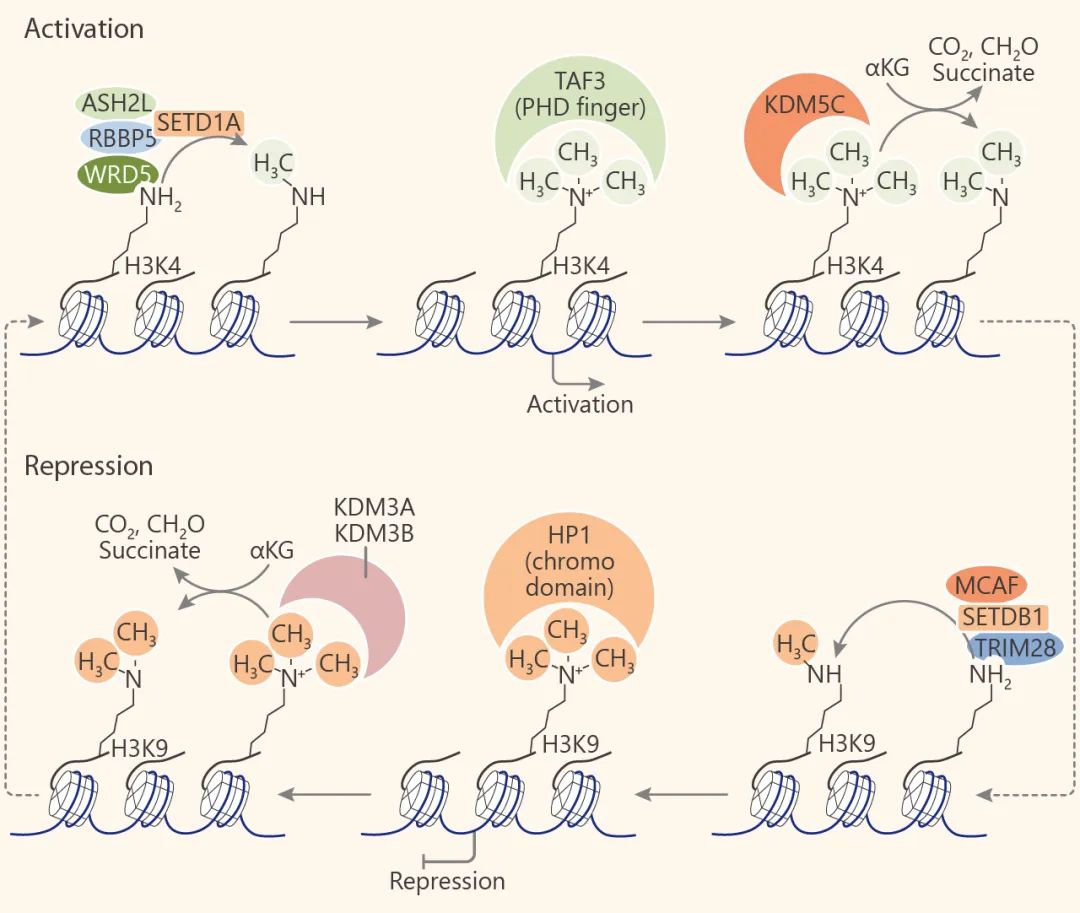
HMTs 和 HDMs 调节基因表达的实例
组蛋白甲基转移酶 (HMTs) 分为两类:赖氨酸甲基转移酶 (KMTs) 和精氨酸甲基转移酶 (PRMTs)。
KMTs 根据催化结构域序列,可分为含 SET 结构域和非 SET 结构域。SET 结构域是组蛋白甲基转移酶的重要结构域,也是大多数转移酶含有的结构域,负责甲基转移酶的酶促活性,包括 SUV39, SET1, SET2, EZH (著名的 EZH2 就在这个家族啦, 可对 H3K27
进行单,二和三甲基化),RIZ (PRDM, SMYD, SUV420) 等家族。而不含 SET 结构域的蛋白较少,如 DOT1L
蛋白。DOT1L 是已知的靶向组蛋白 H3K79 位置的组蛋白甲基转移酶。H3K79 位于组蛋白 H3
的球状结构域中,但它暴露在核小体表面上,在这里它可以被 DOT1L 甲基化。因此,DOT1L 的催化发生在核小体表面而不是 N 末端尾巴上。
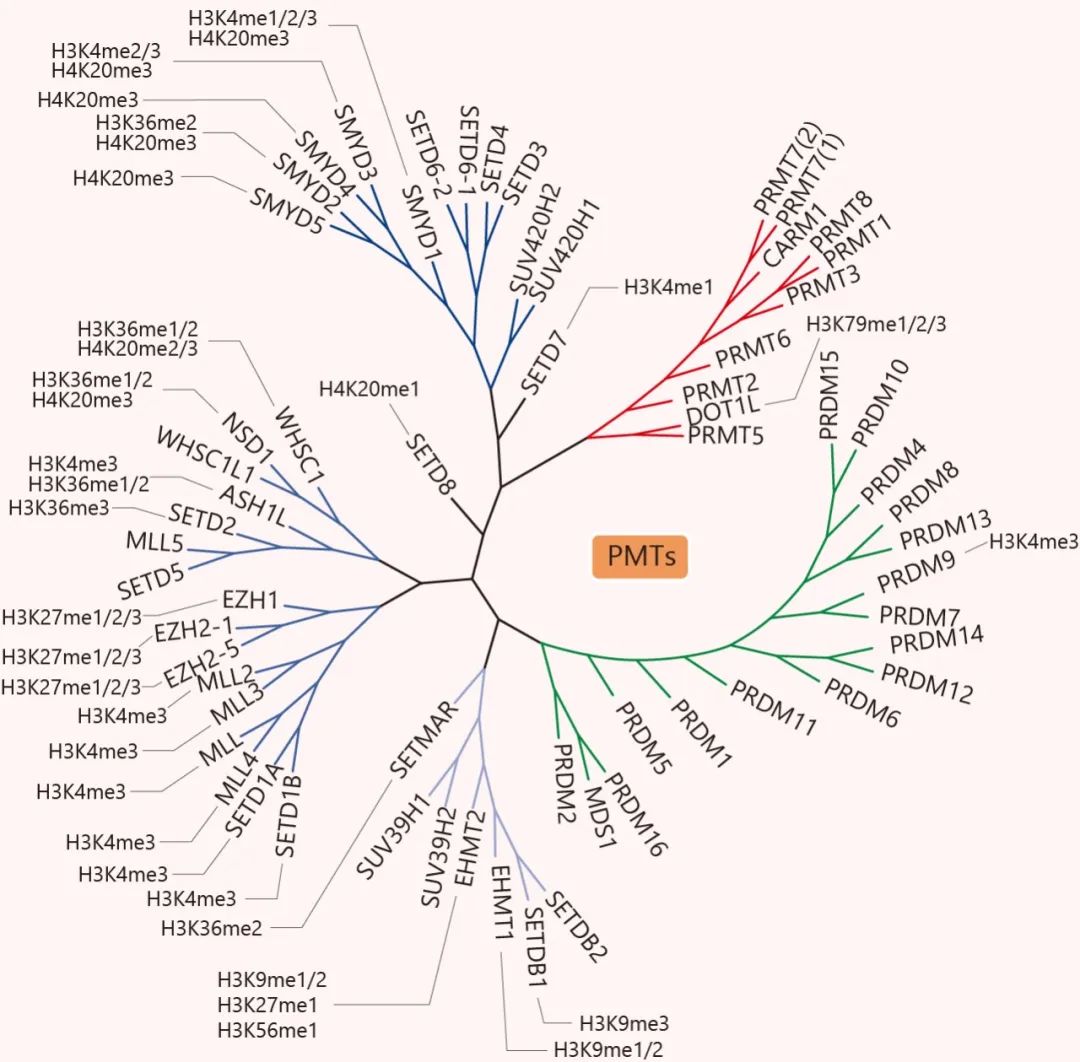
蛋白甲基转移酶的系统发育树
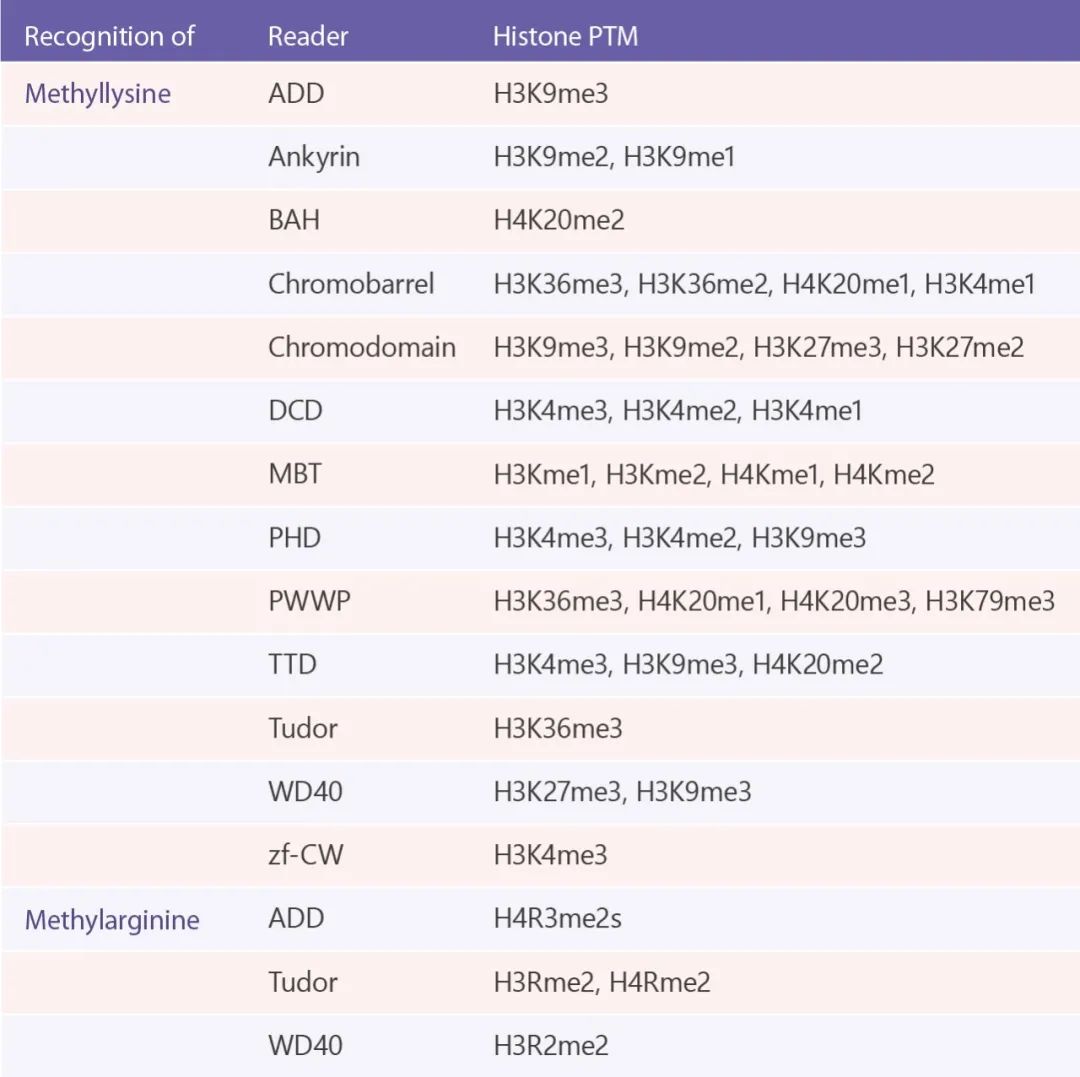
组蛋白甲基化阅读器 (注: PTM: 蛋白翻译后修饰)[10]
如同武林高手组合出招一样,组蛋白甲基化的不同位点和模式可以演化出很多的甲基化修饰模式,增加了受组蛋白甲基化调节的基因表达的复杂性和多样性。而
HMTs 和 HDMs 小心地维持着组蛋白甲基化的水平,因而也就不难理解它们的失调与癌症之间密切的关系,如组蛋白甲基转移酶 NSD1 和
EZH2 在许多肿瘤中过表达,DOT1L 在白血病中有着广泛的作用等等。组蛋白脱甲基酶 KDM1A, KDM5B
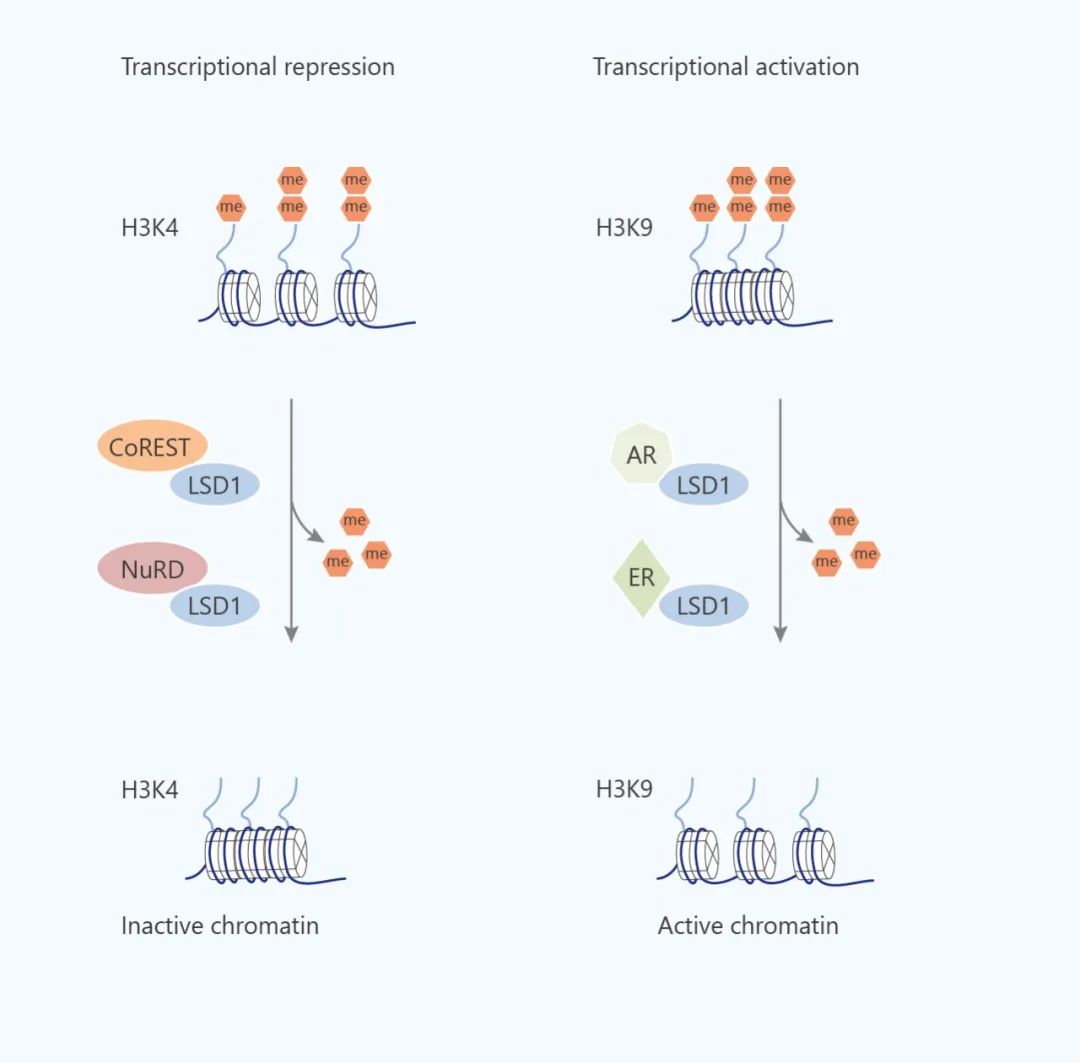
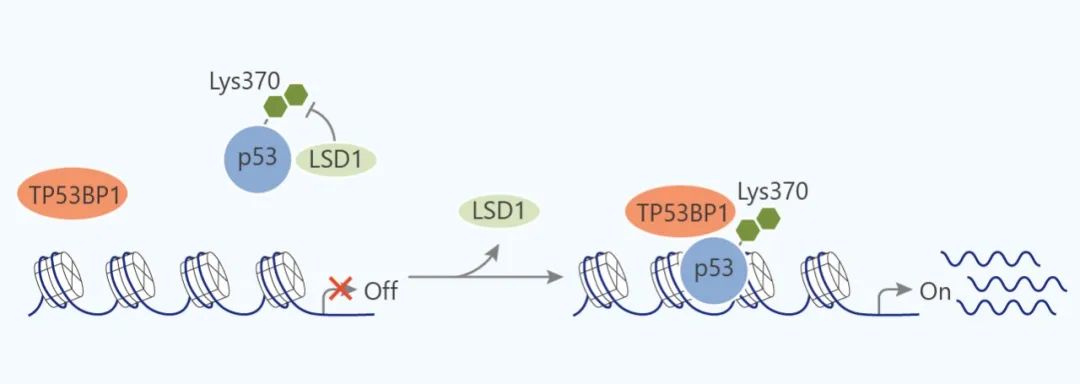
分别在低分化神经母细胞瘤和前列腺癌中过表达。LSD1 与 p53 的直接相互作用会降低 p53 的活性,包括 p21
的表达降低,与肿瘤发生有关等等。另外,对组蛋白甲基化标记的误读 (组蛋白甲基化的读取蛋白活性异常)
也与许多人类疾病有关,包括发育异常以及癌症。因此,这些蛋白质的小分子抑制剂是有用的化学探针或潜在的治疗剂。
部分靶向组蛋白甲基化修饰的蛋白抑制剂
HMTs
选择性,具有口服活性的 EZH2 抑制剂,用于治疗上皮样肉瘤;抑制含有 PRC2 复合体的野生型 EZH2 的活性; FDA Approved
有效的,选择性的 EZH2 甲基转移酶抑制剂;在体内外明显抑制肿瘤形成,降低细胞迁移,侵袭,逆转耐药
有效的,具有选择性的 SMYD2 抑制剂
有效的 DOT1L 组蛋白甲基转移酶抑制剂; Phase 2
有口服活性的 PRMT5 抑制剂
有效的,选择性的,具有细胞活性的人 I 型蛋白精氨酸甲基转移酶 (PRMTs) 抑制剂
HDMs
有效的 H3K27me3/me2 脱甲基化酶 JMJD3/KDM6B 和 UTX/KDM6A 双抑制剂
具有口服活性的,不可逆的 LSD1 抑制剂,具有抗肿瘤活性; Phase 1
有效的 LSD1 抑制剂; Phase 1
是 Jumonji 组蛋白脱甲基酶广谱抑制剂
Reader
L3MBTL1 和 L3MBTL3 的抑制剂
MCE的所有产品仅用作科学研究,我们不为任何个人用途提供产品和服务
缩写:
HMTs: histone methyltransferases
HDMs: histone demethylases
PHD: plant homeodomain
PRMTs: protein arginine methyltransferase
KMTs: histone lysine methyltransferases
DOT1L: Dot1-Like histone methyltransferase
MMA: monomethylarginine
ADMA: asymmetric dimethylarginine
SDMA: symmetric dimethylation
LSD: lysine-specific histone demethylase
KDM: histone lysine demethylases
HP1: heterochromatin protein 1
参考文献
1. Cheng Y, et al. Targeting epigenetic regulators for cancer therapy: mechanisms and advances in clinical trials. Signal Transduct Target Ther. 2019 Dec 17;4:62.
2. Jambhekar A, et al. Roles and regulation of histone methylation in animal development. Nat Rev Mol Cell Biol. 2019 Oct;20(10):625-641.
3. Xin Yi, et al. Histone methyltransferases: novel targets for tumor and developmental defects. Am J Transl Res. 2015 Nov 15;7(11):2159-75.
4. Tian X, et al. Histone lysine-specific methyltransferases and demethylases in carcinogenesis: new targets for cancer therapy and prevention. Curr Cancer Drug Targets. 2013 Jun;13(5):558-79.
5. Michalak EM, et al. s of DNA, RNA and histone methylation in ageing and cancer. Nat Rev Mol Cell Biol. 2019 Oct;20(10):573-589.
6. Kooistra SM, et. Molecular mechanisms and potential functions of histone demethylases. Nat Rev Mol Cell Biol. 2012 Apr 4;13(5):297-311.
7. Milite C, et al. The emerging role of lysine methyltransferase SETD8 in human diseases. Clin Epigenetics. 2016 Sep 22;8:102.
8. Islam AB, et al. Co-regulation of histone-modifying enzymes in cancer. PLoS One. 2011;6(8):e24023.
9. Huang J, et al. p53 is regulated by the lysine demethylase LSD1. Nature. 2007 Sep 6;449(7158):105-8.
10. Musselman CA, et al. Perceiving the epigenetic landscape through histone readers. Nat Struct Mol Biol. 2012 Dec;19(12):1218-27.
11. Zhu H, et al. Molecules. 2020 Jan 29;25(3). pii: E578.Small Molecules Targeting the Specific Domains of Histone-Mark Readers in Cancer Therapy.
12. Albert M, et al. Histone methyltransferases in cancer. Semin Cell Dev Biol. 2010 Apr;21(2):209-20.
13. D'Oto A, et al. Histone demethylases and their roles in cancer epigenetics. J Med Oncol Ther. 2016;1(2):34-40.
14. Arrowsmith CH, et al. Epigenetic protein families: a new frontier for drug discovery. Nat Rev Drug Discov. 2012 Apr 13;11(5):384-400.
15. McCabe MT, et al. Targeting Histone Methylation in Cancer. Cancer J. 2017 Sep/Oct;23(5):292-301.
16. Magliulo D, et al. Lysine-Specific Demethylase 1A as a Promising Target in Acute Myeloid Leukemia.Front Oncol. 2018 Jul 19;8:255
https://m.sciencenet.cn/blog-3506747-1339842.html
上一篇:HPV病毒感染情况和疫苗介绍 - MedChemExpress
下一篇:第二代 HIV-INSTI 的作用方式 - MedChemExpress
全部作者的其他最新博文
- • Canagliflozin 是一种选择性 SGLT2 抑制剂 | MedChemExpress (MCE)
- • DSPE-PEG 2000 是一种 PEG 脂质,可用于形成胶束作为药物递送的纳米颗粒 (MCE)
- • Mosunetuzumab 是一种基于免疫球蛋白G1的人源化双特异性抗体 | MedChemExpress (MCE)
- • Succinyl phosphonate trisodium salt 是一种 α-酮戊二酸脱氢酶抑制剂 (MCE)
- • 甲硝唑是一种具有口服活性的硝基咪唑类抗生素 | MedChemExpress (MCE)
- • ISO-1 是一种巨噬细胞迁移抑制因子 (MIF) 拮抗剂,IC50 为 7 μM (MCE)