博文
《细胞报告》:陆巍/袁逖飞合作解析NMDA受体膜转运在突触可塑性与记忆巩固中的作用
||
北京时间2022年8月16日晚23时,复旦大学/东南大学陆巍研究组与上海交通大学/上海精神卫生中心袁逖飞研究组合作,于Cell Reports在线发表题为“Trafficking of NMDA receptors is essential for hippocampal synaptic plasticity and memory consolidation”的研究成果,对神经元突触后NMDA受体膜转运的功能进行了解析。

NMDA受体是一类主要的离子型谷氨酸受体,在大脑众多生理与病理过程中发挥重要作用。在突触可塑性与学习记忆的细胞模型——长时程增强(long-term potentiation, LTP)中,NMDA受体通常扮演类似“开关”的作用,当外来刺激或经历足以激活NMDA受体后,可造成胞外钙离子经NMDA受体通道内流,继发激活胞内CaMKII等一系列分子,最终造成突触后另一类主要的离子型谷氨酸受体——AMPA受体的膜转运及突触传递的增强,产生NMDA受体依赖的突触可塑性现象。
相对于NMDA受体,AMPA受体介导的电流更容易被激活且幅值较大,LTP通常也是指由AMPA受体介导电流的持续增强现象。而NMDA受体电流相对较小,幅值波动较大,且受体通道内有镁离子的阻塞,通道开放产生电流的阈值也较高,故传统观点认为NMDA受体在突触可塑性的作用主要还是在诱导阶段,突触可塑性诱导后的表达阶段NMDA受体本身活性已不再重要。从1993年开始陆续有研究发现NMDA受体介导的电流也可以产生LTP现象,其主要机制与活动依赖的突触后NMDA受体膜转运有关。那么神经元突触后NMDA受体的膜转运有何生理功能?NMDA受体膜转运是否与AMPA受体膜转运有关?该项研究对这些问题进行了阐明。
该研究首先采用TBS电刺激与甘氨酸灌流这两种经典的LTP诱导方式,在急性海马脑片上分别诱导出AMPA受体电流与NMDA受体电流的LTP,证实这两种LTP可以同时发生,继而证实AMPA受体与NMDA受体的膜转运可以分别介导这两种可塑性形式。当使用一种穿膜短肽Tat-GluA1(L2-3)特异干预PKCλ对AMPA受体GluA1的磷酸化时,可以抑制突触后AMPA受体膜转运及其介导的LTP (AMPA-LTP),但不影响NMDA受体膜转运及其介导的LTP (NMDA-LTP)。这些结果说明特异干预AMPA受体膜转运并不影响NMDA受体膜转运及其介导的可塑性。
突触后NMDA受体从内质网释放后,以NMDA/SAP97复合体的方式向突触后膜转运,当接近突触后膜时,突触后激活的CaMKII磷酸化SAP97的PDZ1区域Ser232位点,造成NMDA受体与SAP97的分离,NMDA受体最终转运上膜。根据这转运过程,研究组先后采用了两种方法抑制NMDA受体膜转运。首先设计了一种穿膜短肽干预NMDA与SAP97的结合,抑制NMDA/SAP97复合体的形成及向突触后的转运。其次,研究组还建立了SAP97的PDZ1区域丝氨酸232点突变小鼠,通过将丙氨酸(Ala)替代该位点的丝氨酸,特异干预CaMKII磷酸化SAP97,抑制突触后NMDA/SAP97复合物的分离及后继的NMDA受体上膜(图1)。研究发现这两种方法均可有效逆转突触可塑性诱导后NMDA受体膜表达的增加,且NMDA-LTP的表达均受到抑制。
值得注意的是,在排除了对AMPA受体与SAP97相互作用的直接影响后,这两种方法可同时抑制AMPA受体膜转运及其介导的AMPA-LTP。这些结果提示在可塑性表达阶段这两种并存的受体膜转运过程中,NMDA受体的膜转运可能起主导作用,NMDA受体膜转运对AMPA受体膜转运可能起调节作用。
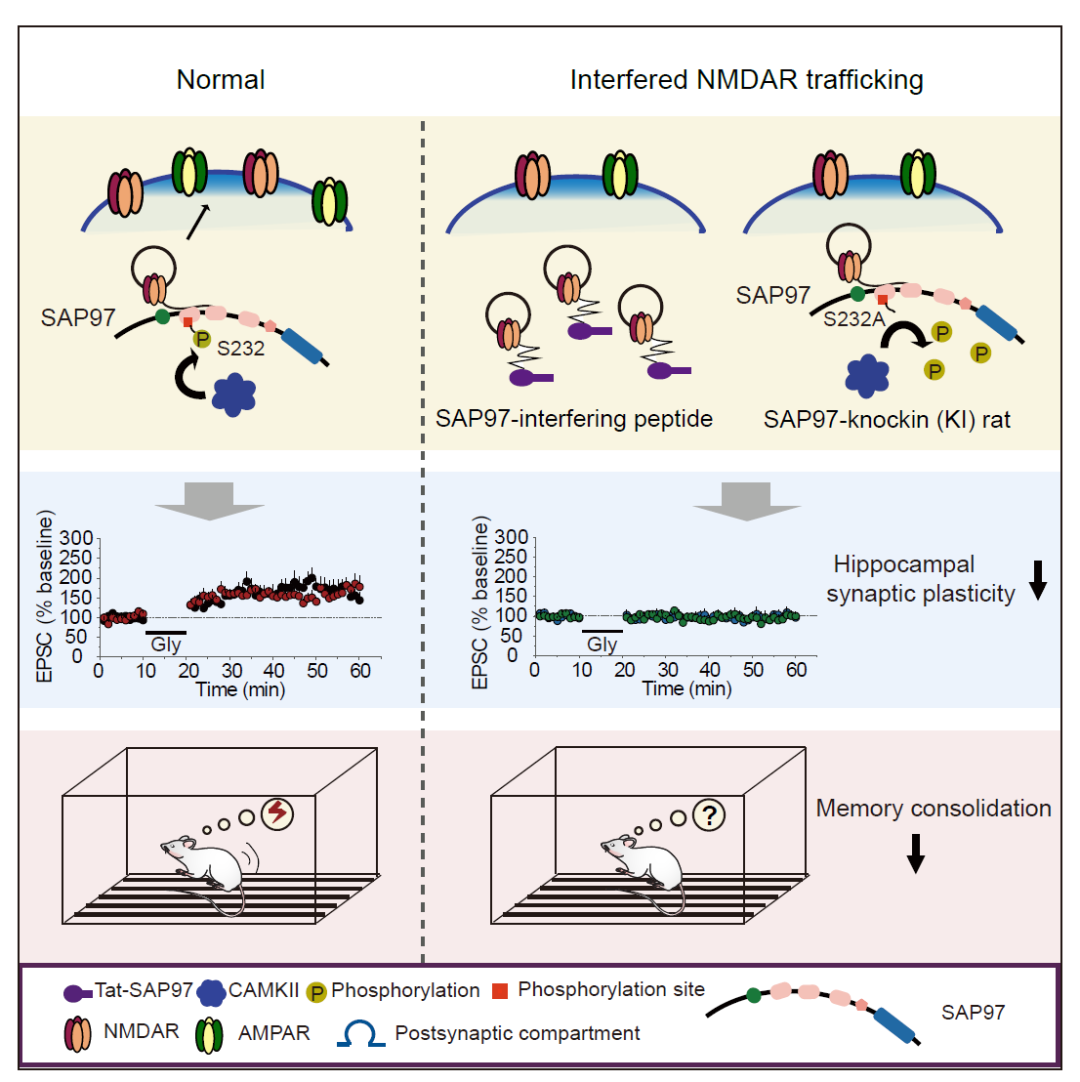
图1. NMDA受体在突触可塑性与记忆巩固中作用的模式及卡通示意图
基于突触可塑性与学习记忆中的重要关系,研究组还观察了NMDA受体膜转运在记忆中的可能作用,发现通过上述两种方式抑制NMDA受体膜转运均能够显著影响场景恐惧记忆的巩固过程。这些结果提示NMDA受体膜转运是突触可塑性与记忆巩固过程所必需的。
NMDA受体膜转运究竟是通过何种分子机制影响了AMPA受体膜转运?是影响AMPA受体转运过程还是影响其上膜后在突触后膜的稳定?通过活细胞动态观察这两种受体的动态转运过程将会是一个有效的方法。然而,由于膜转运的NMDA受体数目远低于AMPA受体,因此需要一种高度敏感高效的分子探针来标记NMDA受体转运带来的细微变化,这也是目前阻碍NMDA受体转运机制研究的一个主要技术瓶颈。
该研究得到国家自然科学基金、科技部科技创新2030重大项目的大力支持。
相关论文信息:
https://doi.org/10.1016/j.celrep.2022.111217
https://m.sciencenet.cn/blog-3423233-1351460.html
上一篇:《自然—方法》:袁瀚等开发基于DNA序列的卷积神经网络单细胞ATAC-seq分析模型
下一篇:《细胞报告》:周专/徐志卿/顾好钢/张勃联合团队揭示可卡因直接调控神经递质分泌