博文
《细胞》:陈建军/苏瑞/夏强团队合作揭示QKI蛋白对mRNA代谢的调控机制
||
北京时间2023年6月27日晚,Cell在线发表了题为 “QKI shuttles internal m7G-modified transcripts into stress granules and modulates mRNA metabolism” 的研究论文,首次揭示了QKI蛋白(Quaking)可以作为mRNA内部m7G修饰的阅读器。QKI特异识别具有m7G内部修饰的mRNA并在应激状态下促进其向应激颗粒(stress granule, SG)内富集,从而调控靶mRNA的稳定性及翻译效率。
美国希望之城国家医疗中心贝克曼研究所的陈建军教授、苏瑞助理教授及上海交通大学医学院附属仁济医院夏强教授为该研究的共同通讯作者,赵之聪博士、卿莹博士和董磊博士为该研究的共同第一作者。

真核生物的信使RNA(mRNA)在其5’端存在帽子结构(7-methylguanosine (m7G) cap, m7GpppN),这一结构对mRNA的剪接、出核转运、稳定性及翻译起始等诸多过程都具有重要作用。近年来的多项研究均证实m7G修饰不仅存在于mRNA的5‘端帽子结构,亦分布于mRNA的内部(mRNA internal m7G modification)。
如芝加哥大学的何川教授课题组于2019年6月报道了一种基于化学转化检测m7G修饰的新测序方法,并利用该技术证实了m7G修饰存在于哺乳动物mRNA的内部,由METTL1-WDR4甲基转移酶复合体催化形成, 相关结果发表于Molecular Cell杂志。同年9月,来自中国科学院北京基因组研究所的杨运桂教授课题组开发了抗体依赖的可在单碱基分辨率上特异性检测mRNA内部m7G修饰的m7G miCLIP-seq测序方法,再次验证了mRNA内部m7G修饰的存在,并发现该修饰可被H2O2及热休克等多种应激刺激调控而影响其修饰的mRNA的翻译效率,相关结果发表于Cell Research杂志。
这些研究结果提示mRNA内部的m7G修饰可被动态调控,但其生物学功能及背后的的分子生物学机制并不清楚。鉴于RNA表观修饰的功能需要由其特异的识别蛋白—阅读器(reader)介导,寻找并鉴定m7G的阅读蛋白对探明其功能及调控靶标mRNA的命运(fate; 比如代谢和翻译)的机制至关重要。
这项最新研究发现,与全细胞裂解液中的其他蛋白相比,QKI蛋白可以选择性结合具有内部m7G修饰的RNA:QKI与具有m7G修饰RNA结合的能力显著高于其与不具m7G修饰RNA的结合能力,且在转录组上的结合基序(binding motif)与METTL1的结合基序及m7G修饰基序高度相似。同时,QKI蛋白可以与应激颗粒组装的核心调控蛋白G3BP1(G3BP stress granule assembly factor 1)结合,在应激状态下携带具有内部m7G修饰的mRNA聚集于应激颗粒中。
对m7G MeRIP-seq、QKI7 RIP-seq、 SG RNA-seq、mRNA stability profiling、polysome profiling等实验结果的综合分析提示受QKI调控的靶基因特别显著地富集于 “Hippo signaling pathway” 和 “pathway in cancer” 信号通路中,且其mRNA的稳定性和翻译效率受到METTL1-m7G-QKI这一信号轴的调控。考虑到多种化疗药物处理均可诱导应激颗粒在肿瘤细胞中的形成,该研究也探索了m7G-QKI信号通路与肿瘤化疗耐药的可能联系,相关的体内外实验结果均表明通过QKI蛋白作为mRNA内部m7G修饰的阅读器可以提高肿瘤细胞对化疗药物如阿霉素的敏感性。
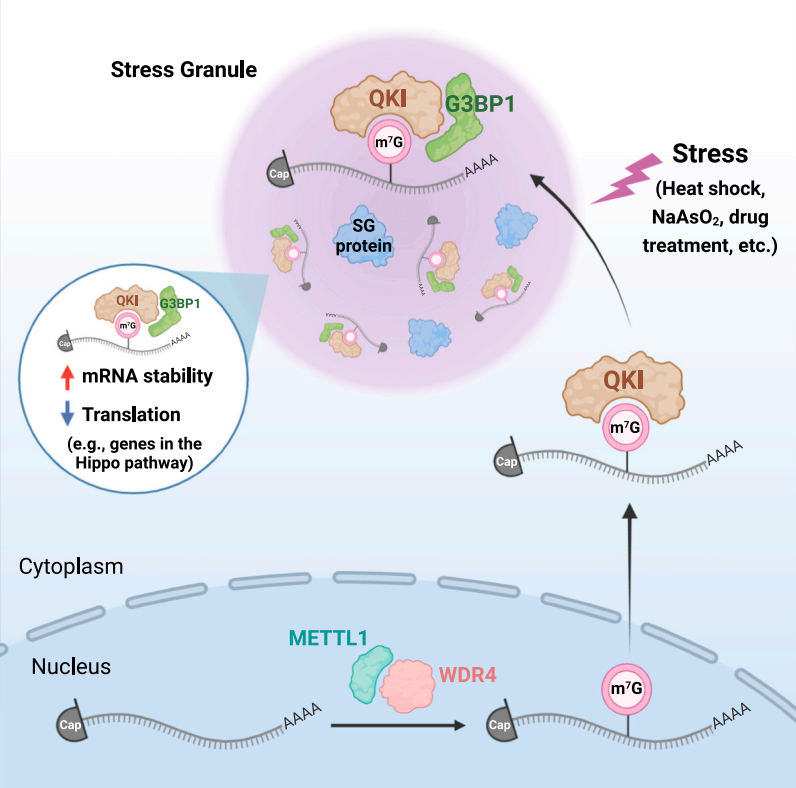
图文摘要
该论文作为首个鉴定mRNA内部m7G修饰阅读器的研究,揭示了mRNA内部m7G修饰与应激颗粒mRNA富集及代谢调控的关系,提示mRNA内部m7G修饰可能具有一系列重要的生物学功能。内部m7G修饰阅读器的成功鉴定为今后深入系统地研究mRNA内部m7G修饰在细胞生长/增殖/分化、细胞周期调控、细胞应激反应、细胞代谢、正常发育、疾病(如癌症)发生/发展、药物应答 (drug response)、以及免疫反应等各种生物过程(bioprocesses)中的作用提供了关键的研究工具及靶标。同时,作为mRNA内部m7G修饰阅读器,QKI本身也可能成为疾病(尤其是癌症)治疗的靶标。
相关论文信息:
https://doi.org/10.1016/j.cell.2023.05.047
https://m.sciencenet.cn/blog-3423233-1393262.html
上一篇:《细胞》:王艳丽团队与合作者发现一种病原微生物感染植物新机制
下一篇:《细胞》:秦为等开发新型邻近蛋白质组学技术TransitID,分析细胞内和细胞间的蛋白动态转运