博文
《分子细胞》:可爱龙/张燕/胡纯一合作揭示Type I-C CRISPR-Cas3系统激活与失活的机制
||
2024年1月18日,美国康奈尔大学可爱龙实验室、美国密西根大学张燕实验室以及新加坡国立大学胡纯一实验室合作在《分子细胞》发表长篇文章,揭开了Type I-C CRISPR-Cas3系统在激活和失活方面的神秘面纱。

科学家的探索之旅,寻找分子世界的开关
在Nla Type I-C系统这个复杂且充满未知的分子世界里,科学家们发现了一个令人兴奋的现象:当Cascade结合靶标DNA之后,Cas3就像是接到了某种神秘的信号,通过与Cas8亚基的“握手”被神秘招募并激活起来。这不仅仅是一个简单的“握手”,更像是一场微观世界的华尔兹舞会,精确而优雅。而另一方面,他们还发现了两个神秘的“反派”角色AcrIC8和AcrIC9,它们能在体内外强力使Type IC Cascade-Cas3系统失活,就像是在这场舞会中突然拉响了警报,让一切都静止了下来。这场在微观世界中上演的“舞会”和“警报”,不仅仅让我们对CRISPR-Cas系统有了更深的理解,也为未来的基因编辑工具开发打开了新的大门。
CRISPR-Cas系统:细菌世界的超级英雄
在细菌和古细菌的世界里,CRISPR-Cas系统就像是他们的超级英雄,保护他们不受外来基因的侵袭。它能够通过可编程的引导RNA序列,对抗那些狡猾的入侵者。而在这个超级英雄家族中,我们已经非常熟悉的Cas9就是其中一员,以其简洁高效而闻名。但是,别忘了,Type I-C系统也是这个家族中的一员,而且它在细菌和古细菌中的分布更为广泛,这意味着它潜藏着更多未被发掘的力量。正是这样一位“隐藏的英雄”,现在终于被科学家们发现并揭示了它的秘密。
《分子细胞》独家揭秘:Type I-C系统的超级能力
接下来,我们一起来看看《分子细胞》杂志是如何揭秘Type I-C系统的超级能力的。从张燕实验室的Type I-C系统筛选工作,到可爱龙和胡纯一实验室的冷冻电镜解析,这一切都像是在进行一场精密的侦探工作。科学家们不仅捕捉到了Cascade和Cas3的每一个动作,还发现了这个系统独特的PAM识别机制。这种“短小精悍”的识别方式,就像是超级侦探在犯罪现场找到了关键的线索。
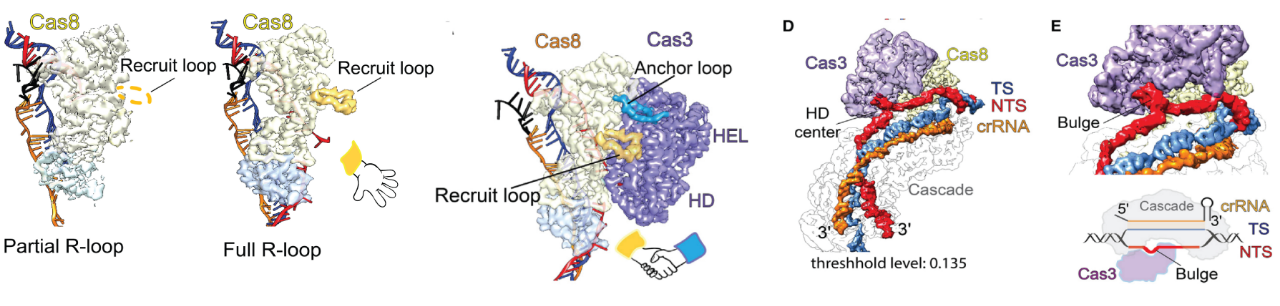
超级英雄遭遇反派:Acr蛋白的出现
但是,每个超级英雄的故事中总会有反派的出现。在这个故事里,Acr蛋白就扮演了这样的角色。张燕课题组通过一系列的实验,发现了AcrIC8和AcrIC9这两个“反派”角色,它们能够巧妙地抑制Cascade-Cas3系统的功能。这就像是在超级英雄的世界中,突然出现了能够削弱他们力量的神秘物质。
结构解析:揭开Acr蛋白的面纱
接着,可爱龙和胡纯一实验室通过深入的结构解析,揭开了这两个“反派”角色AcrIC8和AcrIC9的神秘面纱。尽管他们的结合位置相似,但他们抑制Cascade的方式却截然不同。AcrIC8像是一个策略家,通过空间位置的巧妙运用,迫使Cascade无法识别PAM序列;而AcrIC9则更像是一个伪装高手,通过模仿PAM DNA的结构,巧妙地欺骗了Cascade。这就像是两个高智商的反派,以完全不同的方式达到了同一个目的。
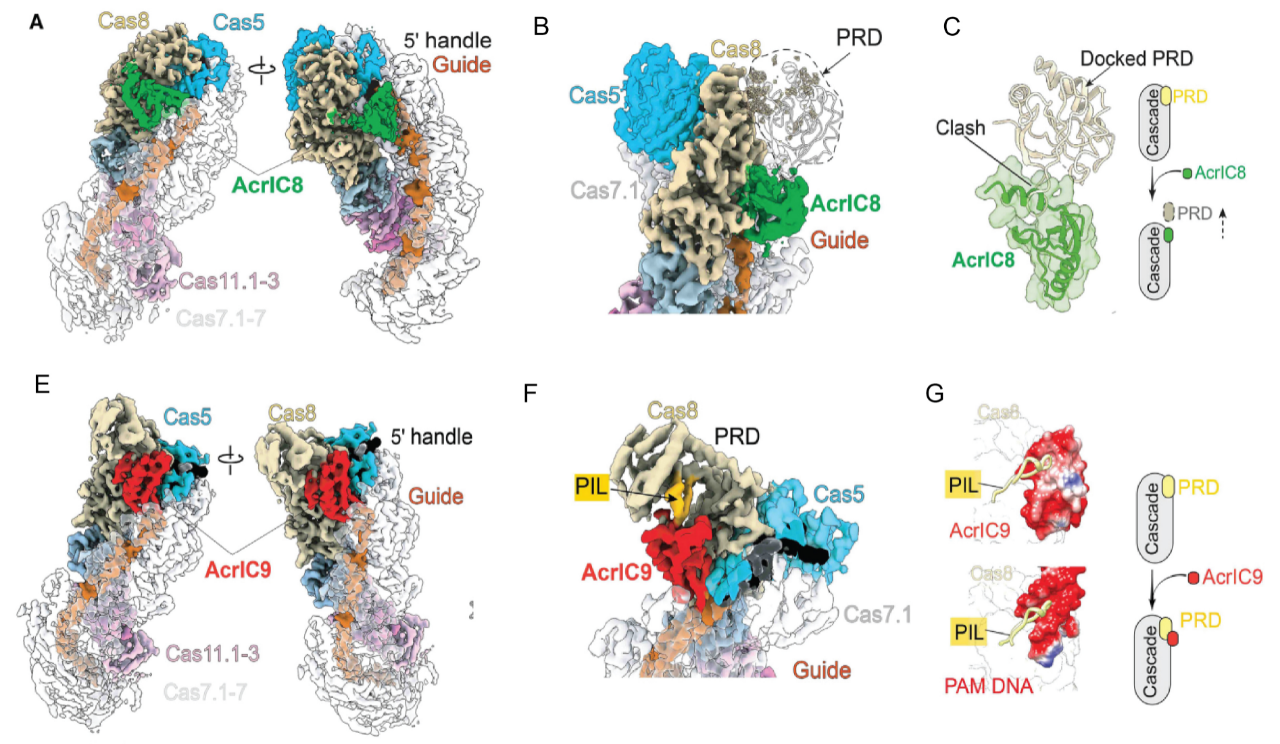
英雄和反派的终极对决:人源细胞中的实验
最终,这场超级英雄与反派的对决延伸到了人源细胞。张燕实验室的研究表明,AcrIC8和AcrIC9不仅在细菌体内有效,而且在人源细胞内也能发挥“刹车”功能,有效地调控Type I-C CRISPR-Cas3系统。这不仅仅是对Type I-C系统功能的一次验证,更是对未来基因编辑和调控工具的一次巨大的启示。
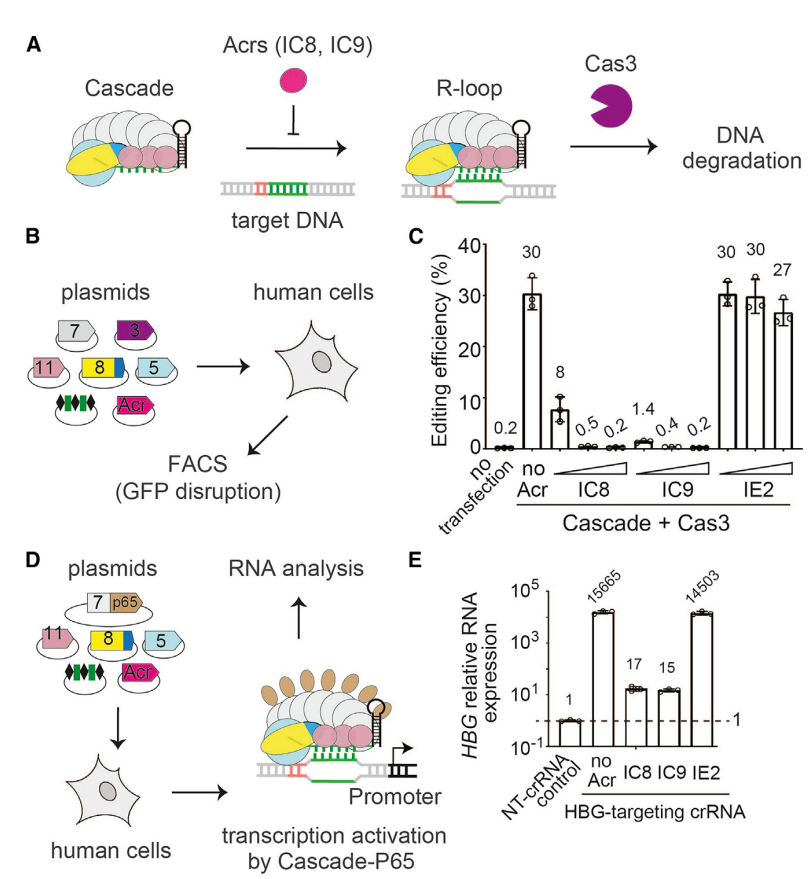
通过这一系列的探索和实验,科学家们不仅揭开了Type I-C CRISPR-Cas3系统激活和失活机制的神秘面纱,更为未来基因编辑技术的发展提供了重要的基础。这不仅仅是一个科学的突破,更是一个关于勇气、智慧和探索的故事。在这个故事中,每一位科学家都是主角,他们用自己的智慧和努力,为人类的未来写下了新的篇章。
相关论文信息:
https://doi.org/10.1016/j.molcel.2023.12.034
张燕教授本科毕业于北京大学生科院,博士毕业于威斯康星大学麦迪逊分校,博士后师从CRISPR领域著名先驱Erik Sontheimer。是最早一批研究Cas9的学者,建立了Type II-C Cas9最全面深入研究以及其在人细胞基因编辑的应用,曾在Cell,Science,Molecular Cell,PNAS 等期刊发表文章。2017年在密歇根大学安娜堡分校建独立实验室,持续深耕于原核生物噬菌体防御及其在真核生物科技上的应用。张燕实验室目前有多个博后职位,欢迎对噬菌体防御和人疾病基因编辑治疗两个方向的有志青年加盟。感兴趣可以联系yzhangbc@med.umich.edu
可爱龙教授早年毕业于中国科技大学,目前于康奈尔大学任教授,获Robert J. Appel Professor荣誉头衔。主攻RNA相关领域的分子机制,包括核酶(Ribozyme)和CRISPR-Cas。在这两个领域都取得了十分喜人的成绩,最近六年发表Nature, Science, Cell论文十余篇。可爱龙实验室目前还有多个博士后名额,欢迎具有生物信息学、细胞生物、基因编辑和结构生物学等背景的优秀博士生申请。感兴趣可以联系:ailongke@cornell.edu
https://m.sciencenet.cn/blog-3423233-1418595.html
上一篇:《自然—遗传》: 中国农业大学徐明良团队报道玉米灰斑病抗病基因ZmWAKL的克隆及其介导的复杂抗病分子机制
下一篇:《自然—结构与分子生物学》:清华大学颉伟团队揭示谱系因子在全能性胚胎中的双向激活功能