博文
《细胞》:张锐 /Alan Brown团队解析衣藻纤毛丝mastigoneme结构,揭开O-糖基化密码
||
北京时间2024年3月28日晚,美国圣路易斯华盛顿大学张锐团队和哈佛医学院Alan Brown团队在Cell杂志发表了题为"Mastigoneme structure reveals insights into the O-linked glycosylation code of native hydroxyproline-rich helices”研究论文。
研究人员用单颗粒冷冻电镜技术解析了衣藻纤毛丝(mastigoneme)的结构,并在其轴心发现了一个新的蛋白。结构显示纤毛丝的两个组分蛋白都有一段富含poly(hydroxyproline) 的区域,此区域包裹了一层“糖衣”。高分辨电镜结构可以鉴定糖衣的组分和与蛋白的连接方式。另外,结构还阐明了纤毛丝和底部PKD通道耦连的分子机制。
这项工作是张锐和Alan Brown团队的第四次合作 (doublet: Cell 2019 【ref1】, radial spoke: NSMB 2021 【ref2】, central apparatus: NSMB 2022 【ref3】, mastigoneme: Cell 2024 【ref4】)。Alan Brown实验室的戴进博士和张锐实验室的马梅生博士(现为华中科技大学教授)是本文的共同第一作者。

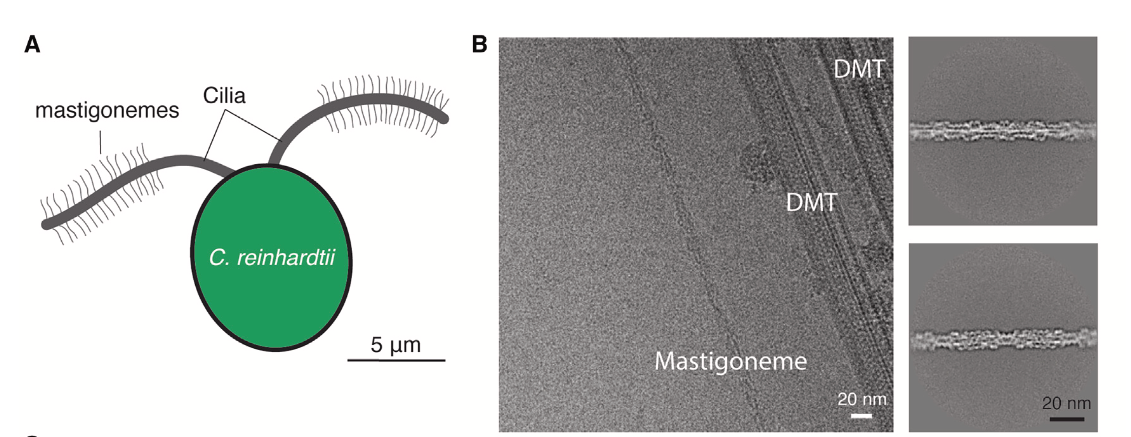
【图1】衣藻的mastigoneme是纤毛表面的毛
在衣藻纤毛轴丝(axoneme)的冷冻电镜照片里,研究团队总是能在背景里看到一些细的filaments。这些filaments后来被证实是纤毛丝mastigoneme,一种藻类和某些原生生物特有的纤毛表面的毛(“毛上毛”)(图1A)。虽然2D average美如画(图1B),但是这个纤毛丝的3D结构解析一开始不是那么顺利,直到团队尝试使用CryoSPARC的ab initio reconstruction才拿到了正确的初始模型(投影能和2D吻合)。这个纤毛丝样品根据定义是一个螺旋结构,但是它的螺旋对称性很不寻常 (rise = 380 Å, twist = 172°)。经过进一步观察团队发现这个结构在螺旋对称性的基础上,在垂直方向还有一个D1对称性(图2)。它的特殊螺旋对称性意味着对于一个颗粒照片,可能需要移动 190 Å才能和模型对上,这已经远远超出了传统软件alignment 的搜索范围。
结构解析的第二个突破是使用了CryoSPARC的helix refine。这个function可以根据 目标结构的螺旋对称性调整照片 alignment的搜索范围, 最终成功达到了3.0 Å的分辨率【图2】。之前文献已知纤毛丝的主要组分是一个叫MST1的糖蛋白(一个1,791 氨基酸的庞然大物)。在这个分辨率下,团队可以trace整个MST1蛋白,并构建原子模型。这个蛋白有9个immunoglobulin-like domain, 一个Cystine rich domain (包含26个二硫键!), 还有一个N端的poly(hydroxyproline) rich region。值得一提的是,在这个工作的投稿准备过程中,耶鲁大学张凯老师也发表了mastigoneme的冷冻电镜结构,阐明了MST1的原子模型【ref5】。
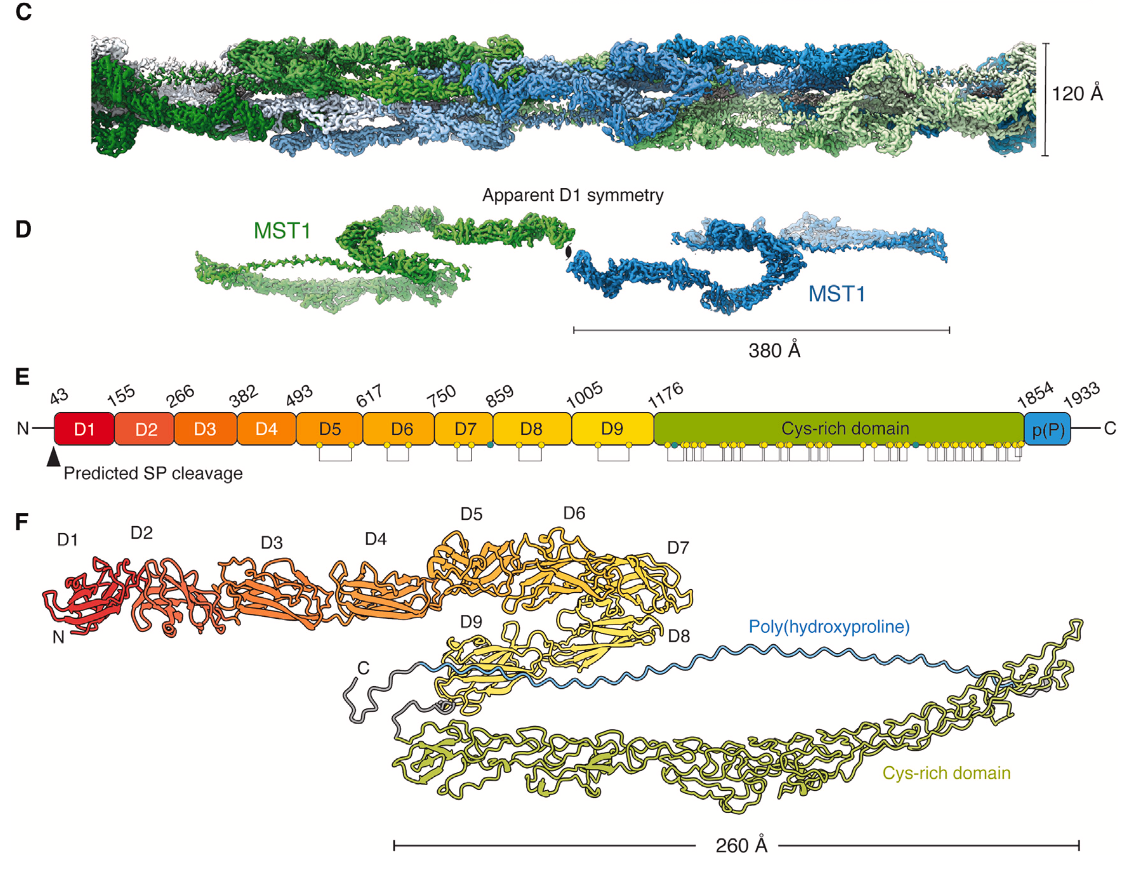
【图2】的MST1组分蛋白的冷冻电镜结构和原子模型
结构显示这个poly-P region 裹着一层"糖衣"(图3A)。在高分辨下可以观测到每个proline(其实是hydroxyproline)都连有glycan 密度,而且是一种不常见的O-糖基化。根据之前为数不多的文献报道,在植物中这种hydroxyproline-rich glycoproteins (HRGPs)主要含有两种糖 组分(L-arabinofuranose and D-galactofuranose)。这两种糖的密度在目前的分辨率下可以区分,并且和密度吻合的很好(图3)。根据这两种糖基的排布和蛋白序列的位置关系(图4),团队总结出了6条基本规律(详情参见正文),在阐明Hydroxyproline-rich glycoproteins (HRGPs)的O-糖基化密码上迈进了一大步(之前的结构研究基本一片空白)。除了O-糖基化, 在MST1蛋白上也可以观测到一些N-糖基化.
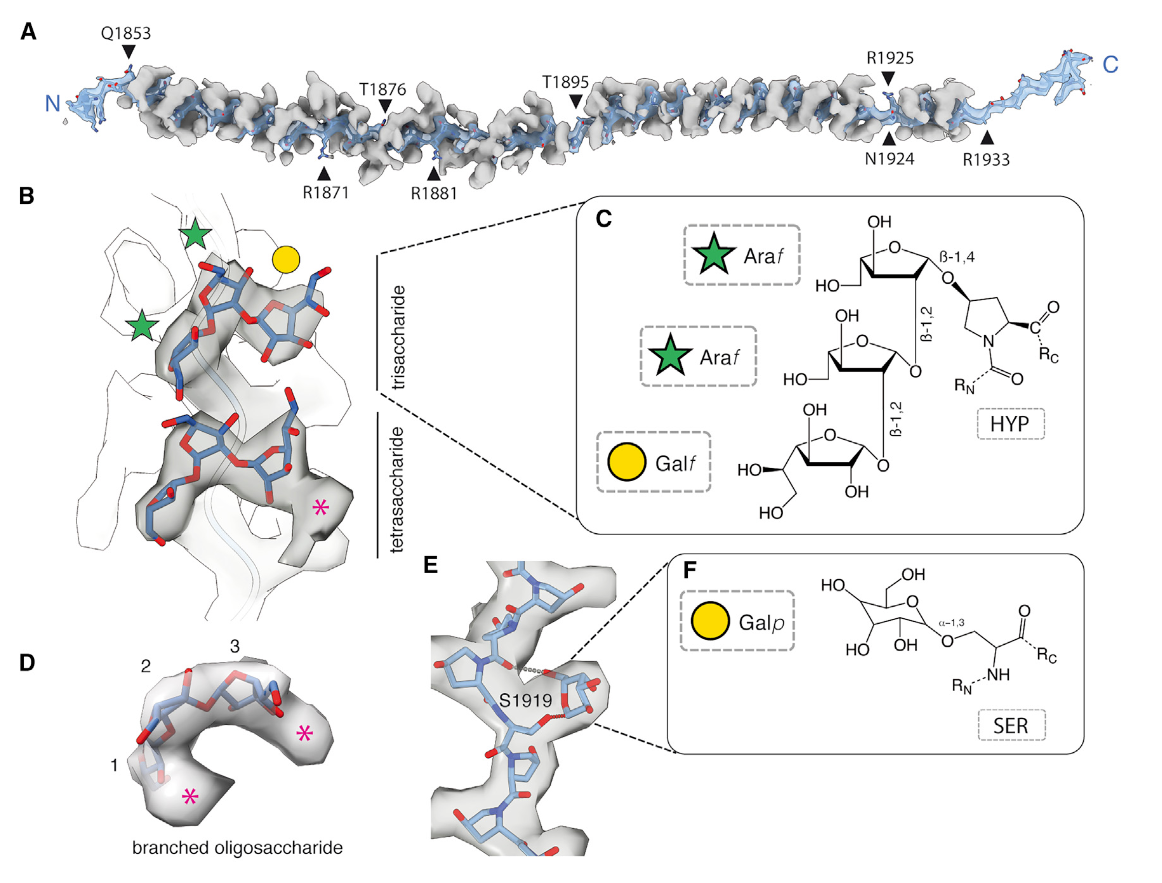
【图3】MST1蛋白的poly-hydroxyproline region上的糖基密度
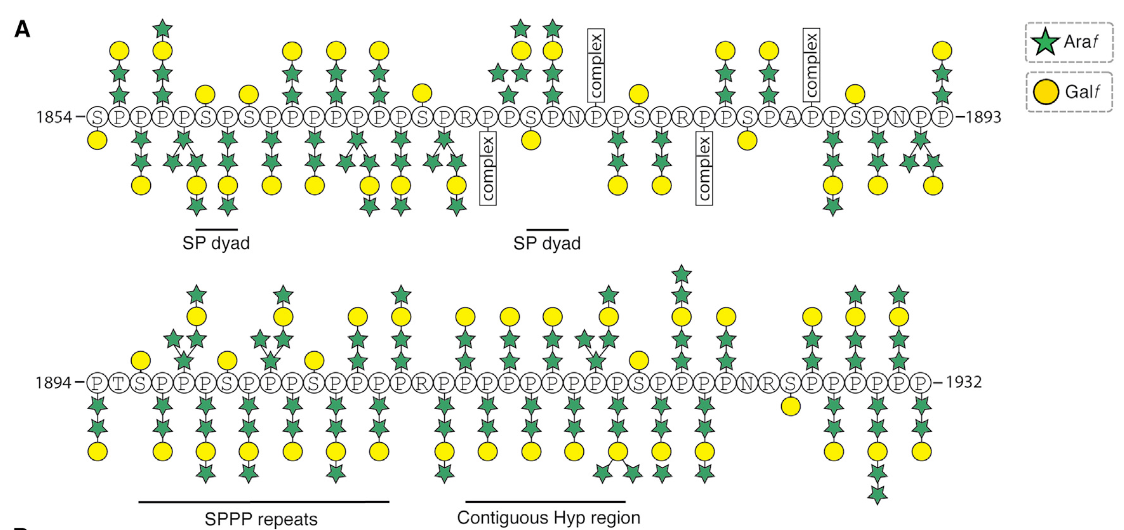
【图4】MST1蛋白的poly-hydroxyproline region上的糖基化pattern
把所有MST1的密度都assign之后,团队发现结构的轴心部分还有一条unassigned 密度(图5)。这些密度会不会属于另外一个蛋白呢?这些密度看着很杂乱,团队猜测这是由于apply了错误的对称性导致的。于是团队把MST1对应的密度从原始颗粒照片里减掉,然后对轴心区域剩余的密度进行3D分类。出来的两个major class果然是D1 对称的,证实了团队的猜测。换句话说,这个filament外圈是螺旋对称性叠加D1 对称性,而轴心却没有任何对称性 (或者说是C1 对称性)。在这个假设下,团队把所有的颗粒从D1对称性revert回C1对称性,从而顺利把轴心区域的密度 解到3.1 Å的分辨率,并且通过侧链密度鉴定出filament轴心确实有另一个蛋白(Cre06.g309951)。团队把这个蛋白命名为MST3,和之前提到的MST1一样,MST3蛋白解析出来的部分也是poly-hydroxyproline rich domain,也裹满了一层糖衣。
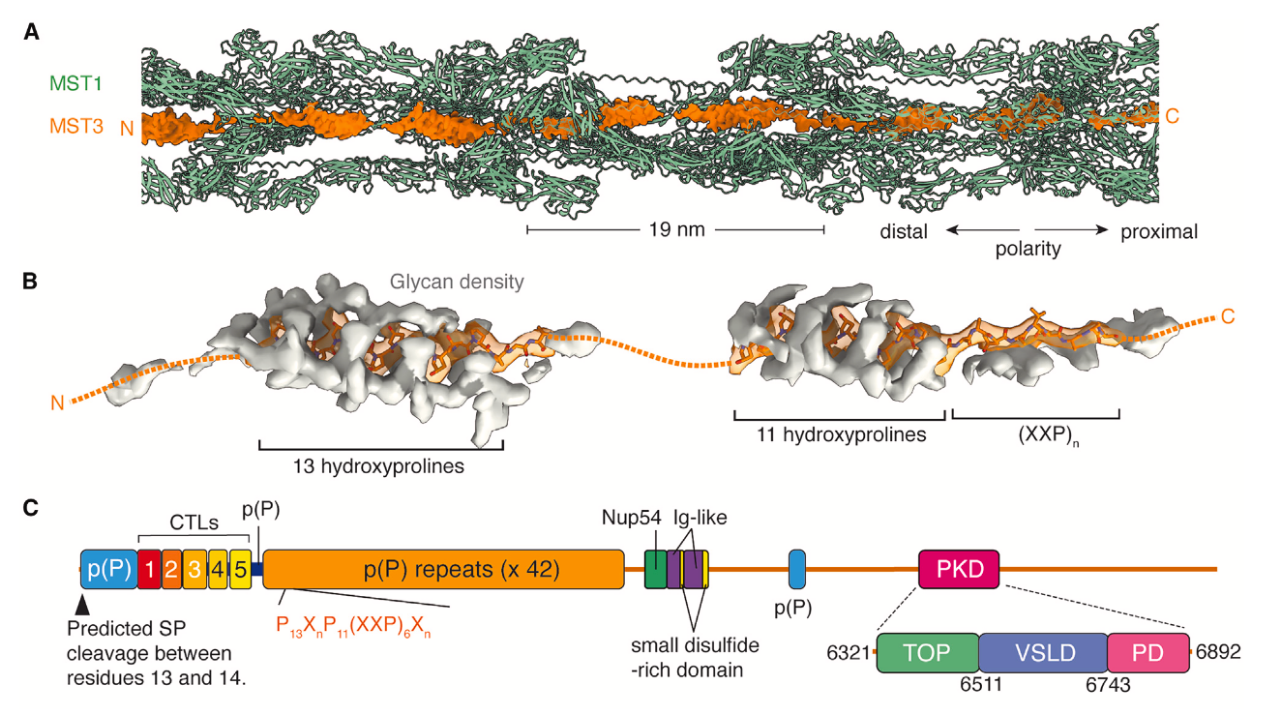
【图5】的轴心是MST3蛋白
如果你觉得之前的MST1蛋白(1,791 个氨基酸)已经是个庞然大物,那么这个MST3蛋白(8,572个氨基酸)简直就是个史前巨兽 。MST3具体大到什么程度呢?整个纤毛丝(总长达800 纳米)从下到上就靠这一个MST3蛋白串起来,并且锚定在纤毛细胞膜上。这个MST3有42个内部重复序列(图5),每个重复序列的蛋白序列均符合P13XnP11(XXP)6Xn的排列规则(pattern),也就是电镜结构里面能看到的这段橘黄色的密度(事实上这个pattern就是靠着电镜结构的密度确定的)。 纤毛丝外圈的MST1的对称性和周期性正好可以和MST3的internal repeat的长度精妙吻合。更有趣的是,这个蛋白的C端有一个PKD-like domain(跨膜区域)。
之前有一篇文献【ref6】报道如果敲除衣藻里的pkd2基因,整个纤毛丝都会随之消失。这篇文章还通过cryo-ET观测到在纤毛丝的基部有一个TRP channel like 密度。PKD1和PKD2在人体内形成PKD channel,是非常重要的TRP家族离子通道。PKD1/2的基因突变会导致一种常染色体显性遗传性多囊性肾病autosomal dominant polycystic kidney disease (ADPKD)。2018年施一公教授在Science上发表首个人源PKD1-PKD2 复合体,在此结构中PKD1和PKD2以1:3的比例形成四聚体【ref7】。目前报道的所有TRP channel基本都是四聚体,但是在体内PKD1和PKD2是否也是以1:3的比例形成TRP channel还存在着一定的争议。这项mastigoneme的工作可以说为1:3比例在体内真实存在提供了一个强有力的证据。为什么这么说呢?首先因为衣藻PKD2蛋白敲除导致纤毛丝消失,那么PKD2应该是其基部channel 的一个组分。同时这个MST3蛋白即是纤毛丝 的组分,C端也有PKD-like domain, 那么MST3 也应该是其基部channel 的一个组分,并且只有一个copy (不然一个channel上就会连着2根以上的纤毛丝)。
综合以上所有的信息,唯一合理的解释就是衣藻的纤毛丝底部的PKD channel 是由MST3和PKD2以1:3的比例组成的(MST3就是衣藻里的那个大家一直寻找的PKD1)。进一步的结构分析和alphafold预测显示MST3的PKD-like domain需要和另一个刚刚发现的SIP蛋白【ref8】组装才能成为PKD channel的一个完整的subunit,并且和PDK2的折叠方式高度相似【图6】。为了验证结构模型,团队对衣藻的mst1,sip,pkd2和mst3突变体做了定量质谱, 结果显示了这些蛋白之间的确存在相互依存关系。在负染电镜下,各种突变体的纤毛上都缺失纤毛丝,也符合预测。此外上述突变体游动速度比较野生型衣藻均有所下降(~15%)。虽然目前衣藻的纤毛丝生物功能还不是很清楚,但是它的摆动产生的mechanical信号有可能通过MST3蛋白传到纤毛丝的基部从而控制PKD channel的开关。这个mechanosensing的机制可能也适用于高等动物的PDK channel。
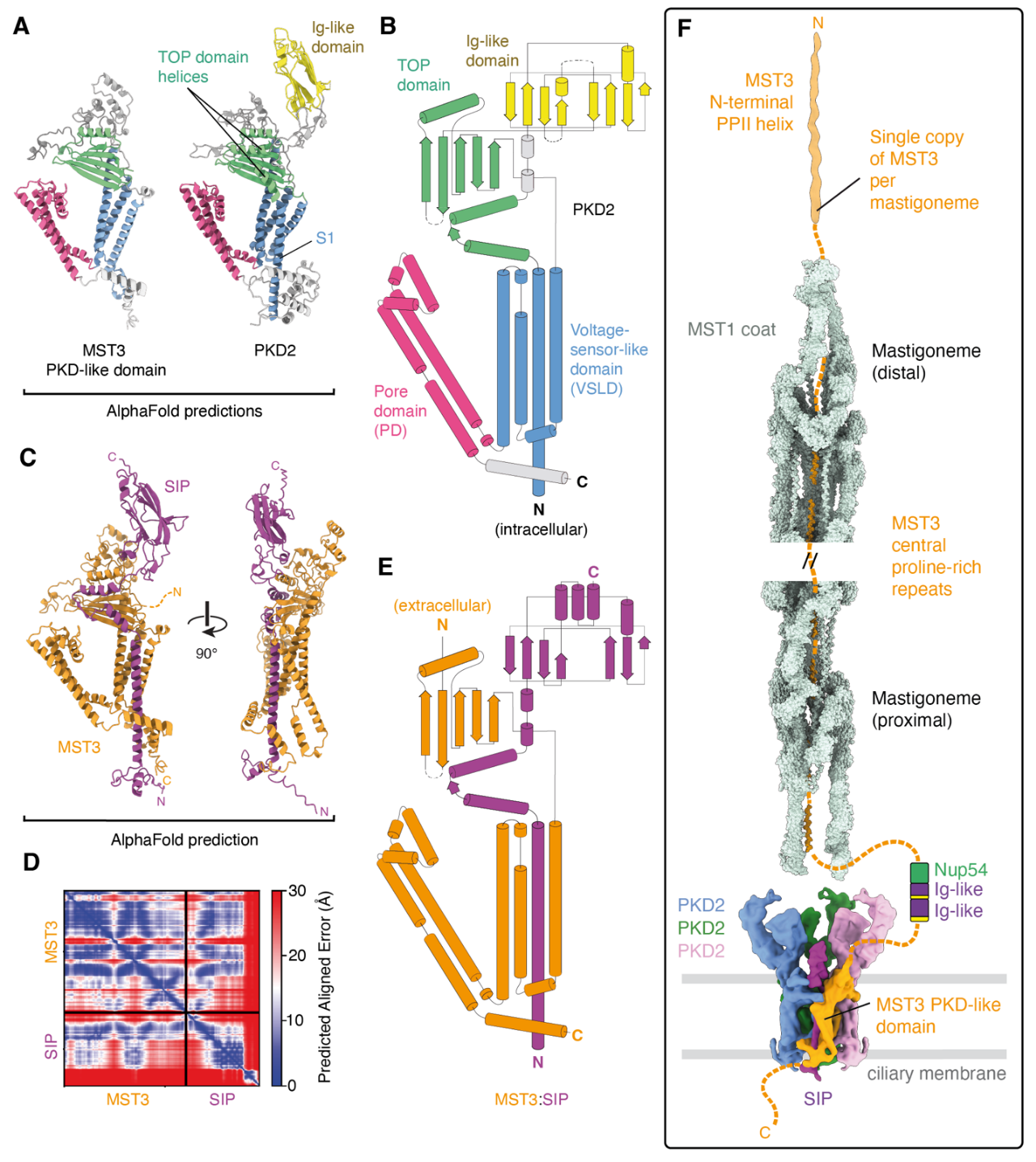
【图6】MST3蛋白参与组装纤毛丝基部的PKD channel
总结,这个例子说明结构生物学可以作为工具发现新蛋白和新机理,然后指导下游的遗传和细胞实验。生物学研究不一定都要假说驱动, 也可以通过观察和学习。做科研没有必要一味追求热点,因为谁也说不准哪片云彩就会下雨。
相关论文信息:
https://doi.org/10.1016/j.cell.2024.03.005
参考文献
1.Ma M, Stoyanova, M, Rademacher G, Dutcher, SK, Brown A#, Zhang R#. Structure of the decorated ciliary doublet microtubule. Cell (2019) 179(4):909-12.
2.Gui M, Ma M, Sze-Tu E, Wang X, Koh F, Zhong ED, Berger B, Davis JH, Dutcher SK,Zhang R#, Brown A#. (2021). Structures of radial spokes and associated complexes important for ciliary motility. Nat Struct Mol Biol 28, 29–37.
3.Gui M, Wang X, Dutcher SK, Brown A#, Zhang R#. (2022). Ciliary central apparatus structure reveals mechanisms of microtubule patterning. Nat Struct Mol Biol 29, 483–492.
4. Dai J*, Ma M*, Niu Q, Eisert RJ, Wang X, Das P, Lechtreck KF, Dutcher S, Zhang R#, Brown A#. Mastigoneme structure reveals insights into the O-linked glycosylation code of native hydroxyproline-rich helices. Cell (online 3/28)
5. Wang, Y. Yang J, Hu F, Yang Y, Huang K, Zhang K#. Cryo-EM reveals how the mastigoneme assembles and responds to environmental signal changes. J. Cell Biol. 222, e202301066 (2023).
6. Liu P*, Lou X*, Wingfield JL, Lin J, Nicastro D, Lechtreck KF#. Chlamydomonas PKD2 organizes mastigonemes, hair-like glycoprotein polymers on cilia. J Cell Biol 219, 386–21 (2020).
7. Su, Q*, Hu F*, Ge X, Lei J, Yu S, Wang T, Zhou Q, Mei C, Shi Y#. Structure of the human PKD1-PKD2 complex. Science 361, (2018).
8. Das P, Mekonnen B, Alkhofash R, Ingle AV, Workman EB, Feather A, Zhang G, Chasen N, Liu P, Lechtreck KF#. The Small Interactor of PKD2 protein promotes the assembly and ciliary entry of the Chlamydomonas PKD2–mastigoneme complexes. J. Cell Sci 137, jcs261497 (2024).
https://m.sciencenet.cn/blog-3423233-1427438.html
上一篇:《自然—生物技术》:王潇团队合成具有核酸外切酶抗性的枝状poly(A)尾,提高mRNA药物稳定性
下一篇:《自然》:浙江大学张国捷团队揭示鸟类辐射演化过程