博文
《自然》: 陈靖/何川/迟洪波合作揭示食物来源血液营养物在抗病免疫中的重要作用
||
北京时间2023年11月23日,芝加哥大学陈靖/芝加哥大学何川/圣裘德儿童研究医院迟洪波团队合作在Nature上发表题为“Trans-vaccenic acid reprograms CD8+ T cells and anti-tumour immunity”的研究论文。该研究利用“血液营养化合物库“筛选出源于反刍动物制品的反式十八碳烯酸(Trans- Vaccine Acid,TVA),揭示其通过促进CD8+ T细胞功能来增强抗肿瘤免疫的机制。
芝加哥大学陈靖教授,芝加哥大学何川教授,圣裘德儿童研究医院迟洪波教授为该文共同通讯作者。芝加哥大学范皓博士,南方科技大学助理教授夏思源,芝加哥大学向俊鸿博士为论文共同第一作者。

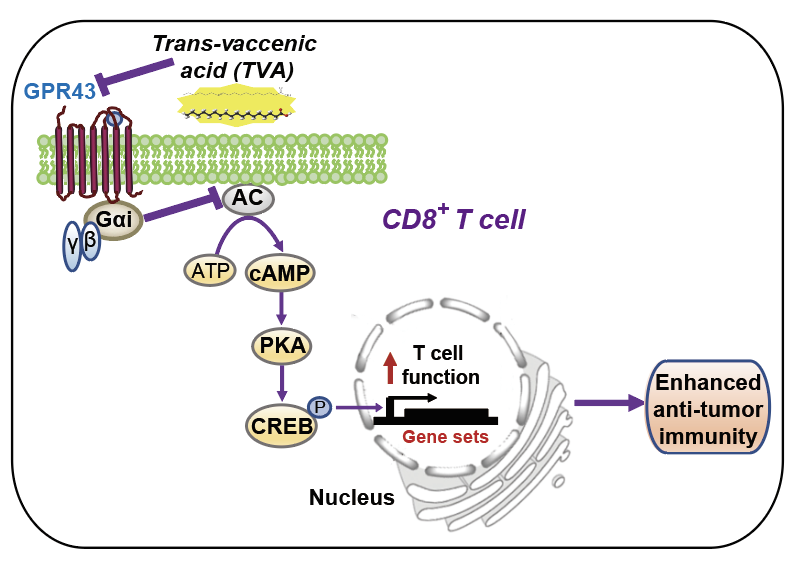
饮食是影响人类正常生理代谢和疾病调控的重要因素。在演化的长河中,人类与环境不断相互适应,人们的饮食结构也在随生理和病理适应的漫长探索中逐渐趋于稳定。因此,人体血液中稳定留存的食物来源营养物无一不是大自然赋予我们的珍宝,它们不单为人体提供能量和用于生物合成的前体物,还起着信号分子的作用,对人体正常生理维持和疾病调控至关重要。 长久以来,人们就饮食与人类健康的联系进行了广泛研究,但由于食物的多样性和饮食代谢的复杂性,导致解释这种联系的机制研究非常困难,目前人们对这些营养物如何影响特定的人体生理和病理进程了解甚少。为解决这一难题,不同于以往着手于食物对人类健康影响的研究,该研究首次总结出大约700种食物来源且可于血液中稳定循环的化合物,并构建了一个包含255种食物来源生物活性分子的“血液营养化合物库“,用于直接解析这些营养物的重要功能。 T 细胞在抗肿瘤免疫中起到重要作用,研究团队首先利用“血液营养化合物库“筛选出能促进T 细胞功能的化合物。通过筛选及一系列验证试验,该团队鉴定出TVA在体外不仅能促进T细胞功能,还能缓解T细胞耗竭。并且在体内试验中,研究人员发现,小鼠日粮中添加TVA能够抑制多种具有免疫原性的肿瘤,然而日粮添加TVA的顺式异构体cis-vaccenic acid (CVA)却没有抗癌效果。另外,去除小鼠CD8+ T细胞后TVA不再具有抗肿瘤效果。进一步分析发现TVA是通过改变肿瘤浸润免疫细胞来起到抗肿瘤效果的,具体来说TVA增加了肿瘤浸润CD8+ T细胞的比例,降低CD8+ T细胞耗竭标志物PD-1和LAG-3,增加了CD8+ T细胞分泌效应分子IL-2,IFN-γ,TNF,GZMB的水平,并促进了其细胞增殖。 图1. 整合时间依赖性机制研究试验设计示意图 接下来该研究团队创新性地进行了整合时间依赖性机制研究(integrated, temporal mechanistic studies),包括:(1) 使用乙氧二羟丁酮辅助的单链DNA测序(the kethoxal-assisted single-stranded DNA sequencing, KAS-seq),通过捕捉细胞全局转录动力学,来识别TVA对CD8+ T细胞的初期影响(20分钟到2小时);(2) 利用磷酸化蛋白组检测(Phospho antibody array)来识别早期阶段的细胞信号变化(40分钟到24小时);(3) 在24小时时,采用RNA测序(RNA-seq)方法进行全转录组分析。该方法完整追踪了TVA从最初接触CD8+ T细胞到引起细胞产生生物学功能变化这一过程中不同阶段的信号改变,以探究TVA影响CD8+ T细胞的机制。结果发现TVA是通过GPCR-CREB通路来调控CD8+ T细胞活性的。进一步试验结果表明,TVA作用于CD8+ T细胞表面受体GPCR来升高cAMP水平,激活PKA-CREB通路,进而调控下游包括Il18, Ebi3, Tbx21, Ilf2, Foxo4, Bcl6等在内的靶基因表达来影响效应CD8+ T细胞功能相关通路,E2F通路,MYC通路等,以起到促进细胞增殖,增强细胞活性,抑制细胞凋亡的效果。值得一提的是,该研究也是芝加哥大学何川教授团队最新发明的KAS-seq方法的首篇时效性应用文章,尤其体现了该方法在捕捉短时间内发生的细胞转录动力学变化的强效性。 图2. TVA调控CD8+ T细胞机制示意图 为了找出TVA的具体靶点,该团队筛选了所有已知游离脂肪酸相关GPCR,成功鉴定出GPR43为TVA的潜在靶点。通过生物学和化学方法,该团队针对TVA进行了结构-活性相关性研究(structure–activity relationship (SAR) studies),通改造TVA和一系列功能试验在体外证明了GPR43是TVA作用于CD8+ T细胞的直接靶点。并进一步运用多种小鼠GPR43敲除模型证明了在体内TVA也是通过GPR43来实现增强CD8+ T细胞功能进而抑制肿瘤的。最后,该研究发现TVA增强了基于T细胞抗癌疗法的效力,包括免疫检查点抑制剂(PD-1/PD-L1 Checkpoint Inhibitors)和双特异性T细胞结合抗体(bi-specific T cell engaging antibody),并提高了嵌合抗原受体(CAR)T细胞的扩增效率。同时也发现对CAR T细胞疗法反应更好的淋巴瘤患者血清中TVA水平更高。 这项工作鉴定出TVA作为食物来源的血液循环营养物在抗病免疫中的重要作用,并通过创新性的机制研究揭示了其作用机理。其具有潜在的临床应用价值,也为后续揭秘食物来源血液循环营养物的众多重要功能打下基础。 相关论文信息: https://doi.org/10.1038/s41586-023-06749-3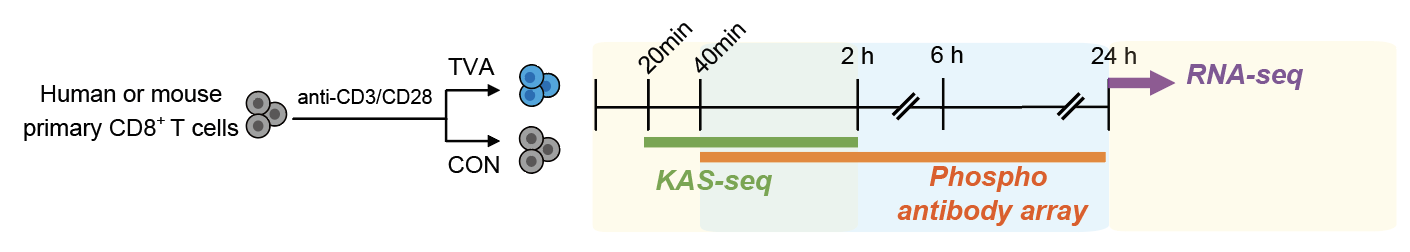
https://m.sciencenet.cn/blog-3423233-1411007.html
上一篇:《自然—方法》:清华大学戴琼海/俞立/吴嘉敏合作开发自监督显微图像增强方法,助力细胞生物学新发现
下一篇:《自然-代谢》:华中科大陈建国/王芳团队发现线粒体裂变驱动神经元代谢负荷促进雄性小鼠应激易感性